올해 급여재평가 대상 7개 성분 중 티옥트산과 프란루카스트, 모사프리드 3개 성분만 급여적정성을 인정받으면서, 약 1700억원 시장이 벼랑 끝에 서게 됐다.
시장규모가 큰 성분들로 전체 시장의 60% 가까이 지키게 됐으나, 나머지 성분들도 블록버스터가 다수 포함돼 있어 제약사들의 타격이 불가피할 전망이다.
건강보험심사평가원은 지난 4일 약제급여평가위원회(이하 약평위)를 열고 2024년 건강보험약제 급여적정성 재평가 심의한 결과를 공개했다.
올해 급여적정성 재평가 대상 약제는 ▲티옥트산 ▲프란루카스트수화물 ▲이토프리드염산염 ▲사르포그렐레이트염산염 ▲레보드로프로피진 ▲모사프리드 ▲포르모테롤 푸마르산염수화물 등 7개 성분이다.
티옥트산 적응증에는 '당뇨병성 다발성 신경염의 완화'와 '당뇨병 다발신경병증의 완화'가 있다. 약평위는 두 적응증 모두 급여적정성이 있다고 판단했다. 대표품목으로는 부광약품의 덱시드정이 있으며, 유비스트 기준 2023년 196억원을 기록했다. 해당 성분 3년 평균 청구금액은 709억원이다.
프란루카스트수화물은 '기관지천식'과 '성인 알레르기비염, 소아 통년성 알레르기비염' 적응증을 갖고 있다. 두 적응증 모두 급여적정성을 인정받았다. 이 성분의 대표품목은 삼아제약의 씨투스정이다. 오리지널은 동아에스티의 오논캡슐로, 삼아제약이 용량을 줄여도 동일한 효과를 낼 수 있게 개선한 정제를 개발해 2016년 개량신약으로 허가 받았다. 2023년 원외처방액 267억원을 기록했으며, 3년 평균 청구금액은 320억원이다.
모사프리드 성분은 '기능성 소화불량으로 인한 소화기 증상(속쓰림, 구역, 구토)'에 쓰이는데, 급여적정성을 인정받았다. 대표품목으로는 대웅제약의 가스모틴과 한국유나이티드제약의 가스티인CR이 있다. 3년 평균 청구금액은 1328억원이다.
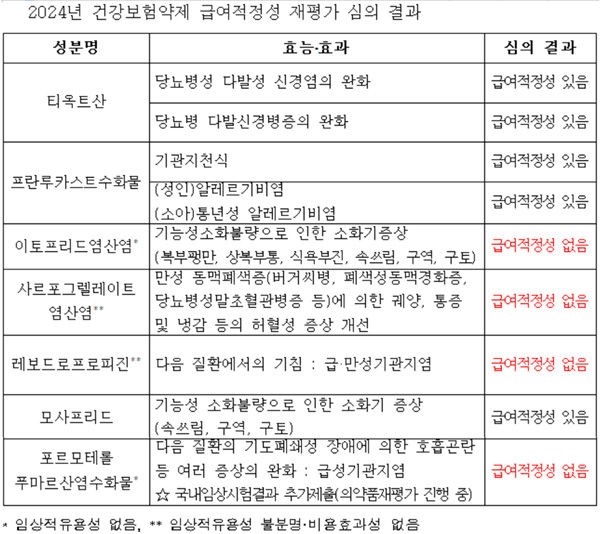
반면 약평위는 나머지 이토프리드염산염과 사르포그렐레이트염산염, 레보드로프로피진, 포르모테롤 푸마르산염수화물 등 4개 성분에 대해 급여적정성이 없다고 결론을 내렸다.
이토프리드염산염은 '기능성소화불량으로 인한 소화기증상(복부팽만, 상복부통, 식욕부진, 속쓰림, 구역, 구토)' 적응증을 갖고 있다. 약평위는 이 성분이 임상적 유용성이 없다고 판단했다. 3년 평균 청구금액은 240억원이다.
사르포그렐레이트염산염은 '만성 동맥폐색증(버거씨병, 폐색성동맥경화증, 당뇨병성말초혈관병증 등)에 의한 궤양, 통증 및 냉감 등의 허혈성 증상 개선'에 쓰인다.
약평위는 이 성분이 임상적 유용성이 불분명하고, 비용효과성이 없다고 봤다. 대표품목으로는 대웅제약의 안플원서방정과 HK이노엔의 안플레이드CR정이 있으며, 2023년 각각 184억원, 176억원을 기록했다. 3년 평균 청구금액은 1109억원이다.
레보드로프로피진은 급·만성기관지염의 기침에 사용되는데, 급여적정성을 인정받지 못했다. 임상적 유용성이 불분명하고, 비용효과성이 없다는 이유에서다. 3년 평균 청구금액은 326억원이다.
포르모테롤 푸마르산염수화물 성분은 '급성기관지염의 기도폐쇄성 장애에 의한 호흡곤란 등 여러 증상의 완화'에 사용된다. 약평위는 임상적 유용성이 없다고 봤다. 현재 이 성분은 의약품재평가가 진행 중이어서, 국내 임상시험 결과가 추가 제출될 예정이다.
이번 급여적정성을 인정받은 3개 성분 시장은 2357억원 규모다. 4개 성분의 급여가 삭제되면 약 1700억원 시장도 흔들릴 수밖에 없을 것으로 보인다.
특히 급여적정성을 인정받지 못한 성분 중 사르포그렐레이트염산염과 레보드로프로피진은 국내사들이 복용횟수를 줄여 편의성을 높였다. 서방형 제제로 개발한 개량신약이어서 논란이 예상된다.
한편 7개 성분 관련 제약사는 결과통보 후 30일 이내에 이의신청서를 건강보험심사평가원에 제출할 수 있으며, 제출된 내용은 약제급여평가위원회의 재심의를 거치게 된다.




![[정책 인사이트] 2027년 지역의사제 속도전…'설계 공백' 논란에도 강행 기조](https://cdn.pharmstoday.com/news/thumbnail/custom/20251126/400494_100525_3125_1763631088_280.jpg)



