케이캡, 나보타 등 향후 3년 내 재심사 기간이 종료되는 431개 품목의 등재특허 정보가 공개된다.
식품의약품안전처(처장 오유경)는 국내 후발의약품(제네릭) 출시 전략 수립에 도움을 주기 위해 향후 3년 동안 의약품 재심사 기간이 종료될 예정인 431개 품목의 등재특허 정보를 공개한다고 30일 밝혔다.
공개되는 품목 정보는 재심사 종료 예정 제품·업체명, 재심사 종료일, 등재특허 유무, 등재특허 만료일 등이다.
또한 시장현황 분석에 참고할 수 있도록 해당 품목의 생산·수입실적과 해당 품목이 속한 ATC코드별 국내 의료보험 급여청구현황과 해외 시장(매출)규모 현황도 함께 제공한다.
이번에 공개되는 431개 품목은 올해 상반기 기준으로 2023~2025년에 재심사 기간 종료가 예정된 의약품이다.
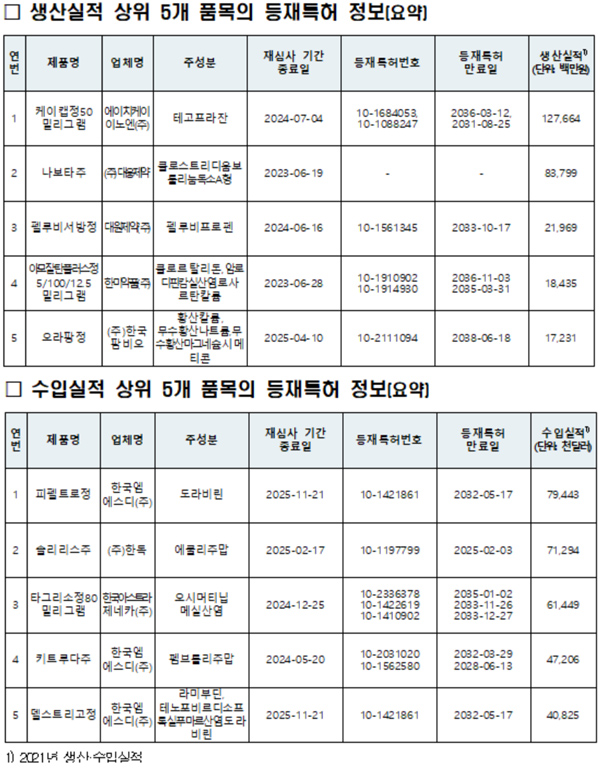
공개 품목 중 국내 생산실적이 200억원 이상인 품목은 ‘케이캡정50밀리그램’ 등 3개 품목이며, 수입실적이 5000만 달러(약 572억원) 이상인 품목은 ‘피펠트로정’ 등 3개 품목이다.
특히 생산·수입실적 상위 각 5개 품목에 대해 등재특허 외에 해당 성분 관련 미등재된 특허정보도 추가로 제공한다.
이번에 공개되는 생산실적 상위 5개 품목의 등재특허 정보에는 HK이노엔의 케이캡정 외에 대웅제약의 나보타주, 대원제약의 펠루비서방정, 한미약품의 아모잘탄플러스정 5/100/12.5mg, 한국팜비오의 오라팡정 등이 있다.
수입실적 상위 5개 품목의 등지특허 정보에는 한국MSD의 피펠트로정 외에 한독의 솔리리스주, 한국아스트라제네카의 타그리소정80mg, 한국MSD의 키트루다주, 한국MSD의 델스트리고정 등이 있다.
식약처는 이번 정보 제공이 국내 후발의약품의 시장 활성화에 도움을 줄 것으로 기대하며, 앞으로도 국내 의약품의 안정적 공급 환경을 조성하기 위해 노력하겠다고 밝혔다.




![[정책 인사이트] 2027년 지역의사제 속도전…'설계 공백' 논란에도 강행 기조](https://cdn.pharmstoday.com/news/thumbnail/custom/20251126/400494_100525_3125_1763631088_280.jpg)



