
정맥임파부전과 치질 치료에 사용되는 광동제약의 '베니톨정'이 불순물 초과 검출로 일부 제품이 자진회수된다. 다만 인체 위해 우려는 매우 낮은 것으로 나타났다.
식품의약품안전처는 혈관보강제로 사용되는 '플라보노이드분획물' 성분 함유 의약품에서 니트로사민계 불순물(니트로소모르폴린, 이하 NMOR)이 일부 제조단위에서 1일 섭취 허용량(127ng/일)을 초과했으나, 인체 위해 우려는 매우 낮은 것으로 확인됐다고 11일 밝혔다.
이번 안전성 조사는 유럽의약품청(EMA)에서 ‘해당 성분이 함유된 의약품에 불순물 NMOR이 1일 섭취 허용량을 초과해 검출된다’는 해외 안전성 정보에 따라 실시됐다.
니트로소모르폴린(N-nitroso-morpholine)은 의약품 불순물 ‘니트로소아민류’ 중 하나로, 주원료에 사용되는 물질인 모르폴린(Morpholine)과 부원료(부형제)에 잔류한 아질산염(Nitrites)이 반응해 비의도적으로 발생하는 것으로 알려졌다.
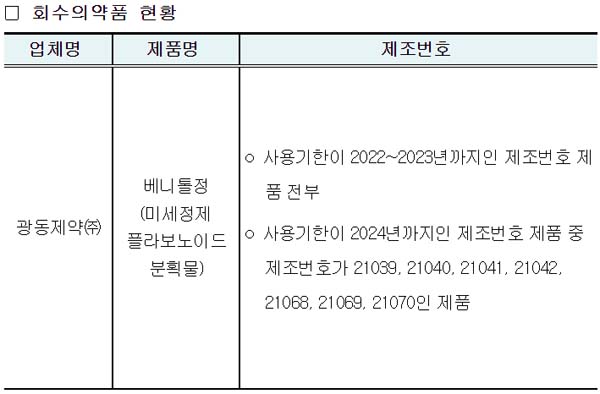
안전성 조사 결과 NMOR 1일 섭취 허용량을 초과한 광동제약의 ‘베니톨정’은 해당 제조업체에서 자발적으로 회수하고 있다.
참고로 지난 2월 17일부터 NMOR이 1일 섭취 허용량 이하로 확인된 제품만 출하하고 있다.
식약처는 해당 의약품 복용 환자들은 임의로 복용을 중단하지 말고 의·약사와 상담 후 복용 지속 여부 등을 결정해야 하며, 필요시 NMOR이 1일 섭취 허용량 이하인 다른 제조번호 제품으로 교환이 가능하다고 설명했다.
식약처는 NMOR의 1일 섭취 허용량을 결정하기 위해 중앙약사심의위원회 자문을 거쳤으며, 의약품 분야 국제 가이드라인(ICH M7)을 적용해 127ng/일로 설정했다.
현재 ICH M7에서는 발암성이 확인되지 않는 변이원성 불순물에 대해 평생(70년)동안 매일 섭취했을 때 ‘무시가 가능한 수준(10만명 중 1명 이하)’을 1일 섭취 허용량으로 정하고 있다. 유럽과 일본에서도 ICH M7을 적용해 NMOR 1일 섭취 허용량을 127ng/일로 정하고 있다.
식약처가 니트로소모르폴린(NMOR) 1일 섭취 허용량을 초과해 검출된 ‘플라보노이드분획물’ 의약품을 복용한 환자의 건강상 영향을 평가한 결과, 전 생애 동안 추가로 암이 발생할 가능성은 ‘무시가 가능한 수준’인 ‘10만명 중 0.382명’으로 나타났다.
식약처는 해당 제품 제조번호를 처방받은 환자들은 의약품 복용을 임의로 중단하지 말고 의·약사와 계속 복용 또는 대체 의약품으로 전환 여부 등에 대해 상담하기를 권고했다.
건강상 우려가 있어 교환이 필요한 경우 남은 의약품을 가지고 조제 받은 약국에 직접 방문하면 다른 제조번호 제품으로 교환을 받을 수 있으며, 해당 의약품을 조제한 약국을 방문할 수 없는 경우 다른 약국에서도 교환이 가능하다. 방문한 약국에서 다른 제조번호 제품으로 교환할 수 없는 경우에는 해당 제약사에 문의하면 된다.
병·의원, 약국에서 해당 제품 제조번호를 처방·조제 시 확인할 수 있도록 3월 11일 오후 2시부터 건강보험심사평가원 의약품안전사용정보시스템(DUR)으로 안내하고 있다.
또한 해당 의약품의 회수·반품이 신속히 이루어지도록 건강보험심사평가원(의약품관리종합정보센터)으로 보고된 ‘플라보노이드분획물’ 함유 의약품의 유통 정보를 해당 제약사, 도매업체, 병·의원, 약국에 제공한다.
식약처는 불순물 NMOR이 1일 섭취 허용량 이하인 ‘플라보노이드분획물’ 함유 의약품만 시중에 공급·유통될 수 있도록 엄격히 관리할 예정이다.
한편 이날 광동제약은 '베니톨정'의 자진회수를 공표하고 일부 제품의 회수 절차에 들어갔다.
회사측은 "보건 당국의 결정에 적극 협조하면서 소비자의 건강과 안전을 최우선 원칙으로 모든 절차를 진행 중"이라며 "이번 회수에 따라 현재 국내에 유통되는 베니톨정은 모두 안전성이 확보된 상태"라고 설명했다.




![[정책 인사이트] 2027년 지역의사제 속도전…'설계 공백' 논란에도 강행 기조](https://cdn.pharmstoday.com/news/thumbnail/custom/20251126/400494_100525_3125_1763631088_280.jpg)



