
국산 코로나19 치료제가 2월 안으로 출시가 가능할까? 이 질문에 대한 답을 쥐고 있는 식약처가 신속심사 과정을 밟고 있는 사이 가능성을 점칠 수 있는 발표가 오는 13일 예고됐다.
엄중식 가천대학교 길병원 감염내과 교수는 대한약학회가 주최하는 '2021 하이원신약개발심포지아'에서 '코로나19 감염 경증~중등증 환자에 대한 렉키로나주의 28일간 치료효과'(Therapeutic Effect of Regdanvimab(CT-P59) in Patients with Mild to Moderate Symptoms of SARS-CoV-2 infection: Day 28 Results from a Multicentre, Randomised Controlled Pivotal Trial)를 발표한다.
이 연구는 셀트리온의 코로나19 항체치료제 렉키로나주(성분 레그단비맙)의 글로벌 임상 2상이다.
셀트리온은 지난해 12월 29일 글로벌 임상 2상을 완료한 후 조건부 품목허가를 신청한 상태다.
렉키로나주는 경증 환자 치료를 목적으로 하는 치료제로 식약처의 신속심사가 완료되는 내달 7일을 기점으로 사용 여부가 결론난다.
앞서 셀트리온은 렉키로나주 승인 후 바로 처방이 가능할 수 있도록 10만명 분량을 만들어낸 상태다.
렉키로나주는 재조합 단백질로 만든 중화 단일 클론 항체로 코로나 바이러스의 스파이크와 결합해 바이러스가 인체 세포내에 침투하는 것을 방지한다. 경증 환자에 사용할 경우 바이러스가 더 이상 퍼지지 않고 회복 될 수 있도록 돕는 역할을 하는 것으로 알려져 있다.
렉키로나주의 2상 임상은 한국, 미국, 루마니아, 영국, 스페인 환자 327명을 대상으로 진행됐으며 이중 한국인은 40명이다.
이번에 발표되는 임상 2상 결과는 한국인을 대상으로 진행된 자료다 .
앞서 셀트리온은 4~5일 내로 코로나바이러스를 죽이고 경증 증상이 있는 환자를 중증 발병으로부터 효과적으로 보호한다고 밝힌 바 있다. 1상에서는 환자의 회복 시간을 44% 단축했다.
대웅제약 역시 코로나19 치료제인 호이스타정(성분 카모스타트메실레이트)에 대한 치료제 사용 여부를 정부와 타진 중이다.
대웅제약 관계자는 "조건부 허가나 긴급사용 승인과 같은 방향을 통해 승인을 받기 위한 작업을 진행하고 있다"며 "정부와 논의를 진행하고 있다"고 밝혔다.
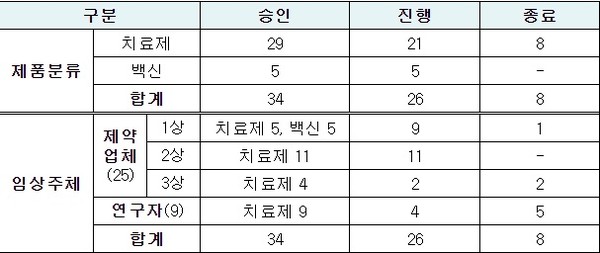
한편 7일 기준 국내에서 개발되는 코로나19 치료제는 29개로 현재 21개 품목이 연구를 진행 중에 있다.
1상을 밟고 있는 치료제는 5개, 2상 중인 치료제는 11개, 3상을 진행 중인 치료제는 9개다.
국산치료제로 연구를 진행 중인 곳은 부광약품(레보비르, 2상), 엔지켐생명과학(EC-18, 2상), 신풍제약(피라맥스, 2상), 종근당(나파모스타트, 2상), 크리스탈지노믹스(카모스타트, 2상), 대웅제약(카모스타트, 2상), 셀트리온(CT-P59, 2상/3상), 제네릭신(GX-I7, 2상), 한국릴리(바리시티닙, 3상), 대웅제약DWRX2003, 1상), 한국MSD(MK-4482, 2/3상), 뉴젠테라퓨틱스(뉴젠나파모스타정, 1상), 동화약품(DW2008S, 2상) 등이다.
셀트리온은 CT-P59(렉키로나주)에 대한 3개 임상을 진행 중이며 1상은 △코로나-19 바이러스 (SARS-CoV-2) 감염 경증 증상이 있는 시험 대상자에서 CT-P59의 안전성, 내약성 및 바이러스학을 평가 △경증 또는 중등증 코로나-19 바이러스(SARS-CoV-2) 감염 환자를 대상으로 표준 치료와 병행하여 CT-P59의 유효성 및 안전성을 평가 △코로나-19 바이러스(SARS-CoV-2) 감염 환자와 접촉한 시험 대상자에서 CT-P59의 예방적 유효성, 바이러스학 및 안전성을 평가하는 임상을 진행 중에 있다.
셀트리온이 진행하는 임상이 모두 허가를 받을 경우 렉키로나는 경증환자 치료는 물론 중증 환자 치료에도 사용할 수 있게 되며 백신을 대체한 코로나19 예방 목적 의약품으로도 사용될 수 있다.




![[정책 인사이트] 2027년 지역의사제 속도전…'설계 공백' 논란에도 강행 기조](https://cdn.pharmstoday.com/news/thumbnail/custom/20251126/400494_100525_3125_1763631088_280.jpg)



