빈혈 부작용으로 현재 FDA 승인을 받은 골수섬유증 치료제의 적합성에 대한 우려가 제기됐지만, 최근 몇 년 동안 관련 약물에 대한 미국 FDA에서 희귀의약품 지정(ODD) 수가 급증했다.
데이터 및 분석 회사인 글로벌데이터에 따르면, 2014년 이후 총 11개의 ODD가 허가됐고, 이 중 8개가 2020년 이후에 지정됐다.
골수섬유증은 골수에 흉터 조직이 축적되는 공격적인 혈액암이다.
이렇게 축적된 흉터 조직은 인체의 정상적인 혈구 생성을 방해한다.
미국 NORD(National Organization for Rare Disorders)에 따르면, 골수섬유증은 미국에서 매년 인구 10만 명당 약 1.5명의 환자가 발생하는 희귀 질환이다.
높은 수준의 ODD 허가는 골수섬유증 내에서 미충족 욕구를 해결하기 위해, 대안적인 작용 메커니즘을 탐색하기 위해 FDA가 중점을 두었음을 보여준다고 글로벌데이터가 평가했다.
현재 이 질환에 대해 FDA 승인을 받은 혁신적인 약물은 4개로, 모두 JAK(Janus kinase) 억제제이다.
골수섬유증 치료에 효과적이지만, 이 작용기전은 전신의 산소 순환을 감소시켜, 빈혈 증상을 유발하고 악화시킬 수 있는, 골수억제로 잘 알려져 있다.
약 절반의 환자가 이미 빈혈 진단을 받고 있기 때문에, 이 환자 집단에게 이익이 되는 승인된 골수섬유증 치료제에 대한 중요한 욕구가 있다.
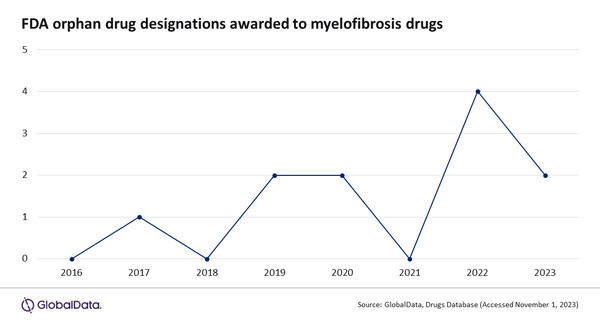
2020년 이후, 8건의 ODD가 FDA에서 허가돼, 지난 4년보다 2배 이상 증가했다.
2022년 FDA에서 허가한 ODD 수는 4건으로, 각각 2건인 2019년과 2020년의 이전 최고 연도와 비교해 2배 이상 증가했다.
2014년 이후 FDA에서 ODD를 받은 12개 골수섬유증 치료제 중 2개만이 JAK 억제제이다.
이는 빈혈 유발 작용 기전에서 벗어나 FDA의 규제 초점이 바뀌고 있음을 보여주는 사례라고 글로벌데이터가 밝혔다.
비슷한 작용 기전을 공유하는 2개 약물을 제외하고, 나머지 10개의 치료제는 다양한 치료 기전을 갖고 있다
MSD의 리블로질(Reblozyl,luspatercept)은 GFD(growth/differentiation) 11과 8 억제를 통해 작용한다.
이 재조합 융합 단백질은 2020년 1월 FDA에서 ODD 허가를 받아 빈혈 관련 골수섬유증에 3상 연구에 있다.
FDA의 최근 ODD 허가 증가는 빈혈을 유발하거나 악화시키지 않는 작용 기전을 특징으로 하는 새로운 골수섬유증 치료제의 개발을 촉진하기 위한 노력의 강화를 강조한다.
지정 허가의 이런 증가는 골수섬유증 치료의 미충족 영역과 관련해 더 많은 이점을 제공하는 더 많은 치료제의 승인으로 이어질 수 있다고 글로벌데이터가 밝혔다.




![[정책 인사이트] 2027년 지역의사제 속도전…'설계 공백' 논란에도 강행 기조](https://cdn.pharmstoday.com/news/thumbnail/custom/20251126/400494_100525_3125_1763631088_280.jpg)



