
초기 유방암 치료에 CDK4/6 약품의 경쟁에 가열되고 있다.
가장 최근, 노바티스는 릴리에 도전하는 유방암 치료제 키스칼리(Kisqali)의 시장 잠재력을 유의하게 확대할 수 있는 긍정적인 데이터를 발표했다.
3상 NATALEE 연구의 톱라인 데이터에서, 노바티스의 키스칼리(ribociclib)가 초기 유방암의 재발 위험을 줄이는, 1차 최종목표를 충족했다고 밝혔다.
구체적인 데이터는 밝히지 않았지만, 키스칼리와 내분비 요법의 복합은 표준 보조 내분비 요법 단독과 비교해, HR+/HER2- 유방암 환자에서 침습적 질병 없는 생존(iDFS)을 유의하게 개선했다.
NATALEE는 이미 목표를 도달했기 때문에, 독립 데이터 모니터링 위원회(IDMC)는 연구를 조기에 종료할 것을 권고했다.
긍정적 데이터는 키스칼리를 전이성 유방암에서 초기 질병의 보조 세팅으로 이동시킬 수 있다.
노바티스의 승리는 릴리의 라이벌 약물인 버제니오(Verzenio)에 직접적인 위협이다.
2021년 버제니오는 HR+. HER- 초기 유방암에 대한 보조 요법으로 승인된 첫 CDK4/6 억제제가 됐다.
지난해 12월 샌안토니오 유방암 심포지엄 2022 미팅에서 발표된 3상 monarchE 임상에서, 내분비 요법에 버제니오 복합은 고위험 환자의 질병 재발 또는 사망 위험을 25.3% 줄였다.
최근 미국 FDA는 버제니오 환자를 선택하기 위해 바이오마커 점수 요건을 제거함으로써 적응증을 확대했다.
하지만, 버제니오는 일부 림프절 관련이 있는 재발 위험이 높은 환자에게만 여전히 승인됐다.
반면, 키스칼리의 NATALEE 임상시험은 또한 중간 위험 환자도 포함됐고, 결절 상태에 관계없이 2, 3기 초기 유방암에 대한 지속적인 이익을 보고했다.
노바티스는 이런 데이터가 재발을 예방하기 위해 우수한 내성 옵션이 제한되어 있는 결절 관련이 없는 환자 등, 재발 위험이 있는 환자에 대해 패러다임을 바꿀 수 있는 잠재력을 가지고 있다고 보도자료에서 언급했다.
monarchE와 NATALEE 연구 모두에서 환자의 생존 결과는 미완성이었다.
보조 적응증은 화이자의 입랜스(Ibrance) 등, CDK4/6 억제제 사이에서 버제니오의 시장 점유율을 높였다.
입랜스는 이런 보조 세팅을 돌파하려는 시도가 실패했다.
2022년 12월, FDA는 폐경 상태에 관계없이 HR+/HER2-전이성 유방암 치료에 아로마타아제 억제제와 입랜스의 병용요법에 대해 적응증을 확대를 승인했다.
현재, 입랜스는 폐경 상태에 관계없이, 아로마타제 억제제 또는 풀베스트란트(fulvestrant)와 복합으로 HR+/HER2- 전이성 유방암 치료에 FDA 승인을 받은 유일한 CDK 4/6 억제제이다.
CDK4/6 억제제가 고위험 코호트에 긍정적 결과를 입증할 경우, 상업적 기회에 영향을 미칠 것으로 예상된다.
매출
키스칼리의 경우 전이성 유방암에 확실한 데이터에도 불구하고, 노바티스의 약품은 매출이 뒤처져 있다.
2022년 노바티스는 연간 31% 급증한 12.3억 달러의 키스칼리 매출을 보고한 반면, 릴리의 버제니오 매출은 24.8억 달러로 전년대비 84% 급등했다.
화이자의 입랜스 매출은 51.2억 달러로 6% 떨어졌다.
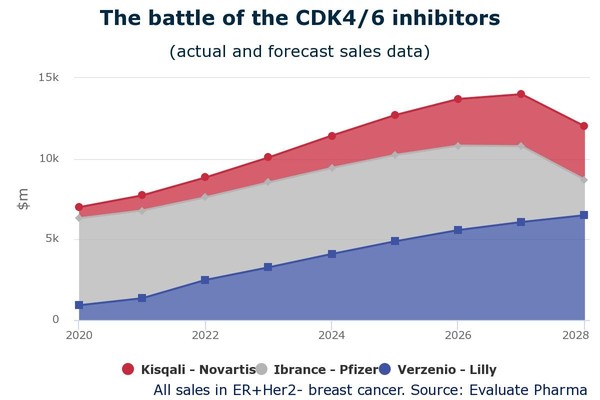
리서치 업체인 EP(Evaluate Pharma)에 따르면, 노바티스의 키스칼리 매출은 2028년 33억 달러에 도달할 것으로 예상된다.
릴리의 버제니오 매출은 2023년 32.6억 달러, 2028년 약 65억 달러로 2배 성장할 전망이다.
반면, 화이자의 입랜스 매출은 2026년 52.3억 달러로 정점에 도달한 후, 2027년 약 47억 달러, 2028년 22억 달러로 급감할 것으로 추정된다.




![[정책 인사이트] 2027년 지역의사제 속도전…'설계 공백' 논란에도 강행 기조](https://cdn.pharmstoday.com/news/thumbnail/custom/20251126/400494_100525_3125_1763631088_280.jpg)



