GSK 긍정적 2/3상 연구결과 3상 임상 선두로 부상
노바티스, 릴리 등 각축전…첫 성공 위해 유망한 데이터 필요
TIM-3는 체크포인트 수용체이며 면역 종양학 분야에서 주목을 받는 일련의 타깃 중 가장 새로운 것 중 하나로, 일부 바이오텍과 제약사들이 개발을 위해 경주하고 있다.
로슈 후보의 실패 이후 다른 체크포인트 수용체인 TIGIT에 대한 관심과 함께, TIM-3는 현재 각광을 받을 수 있게 됐다.
하지만, 개발 업체들은 이전의 최신 면역 종양 표적의 불운한 운명을 피할 수 있음을 보여주기 위한 데이터가 필요하다.
최근, GSK는 2/3상 비소세포 폐암(NSCLC) 임상시험의 두 코호트가 다음 단계 임상으로 진행하기 위한 기준을 충족했다고 밝혔다.
첫 번째 코호트의 환자들은 항 TIM-3 항체 코볼리맙(cobolimab), GSK의 PD-1 체크포인트 억제제 젬퍼리(Jemperli), 화학요법 도세탁셀(docetaxel)을 받았다.
두 번째 코호트의 참가자들은 젬퍼리와 도세탁셀만 받았고, 세 번째 그룹은 대조군으로 도세탁셀 단독요법을 받고 있다.
GSK는 아직 임상 2상 부분의 데이터를 공개하지 않고 있다.
이번 결과로 GSK는 TIM-3 경주에서 선두를 지켰다.
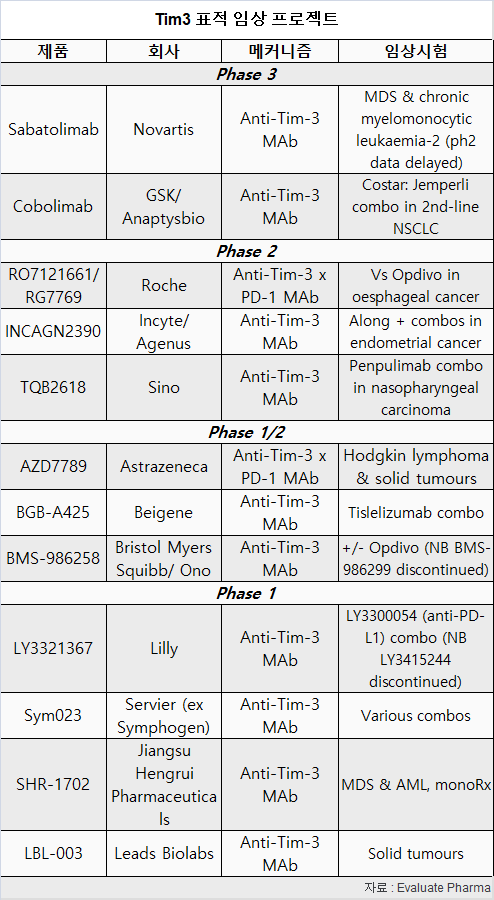
Tim3 경주는 3상 임상에서 기술적 리더로서 노바티스의 사바톨리맙(sabatolimab)이 앞서 있지만, 로슈의 빠르게 진전되는 RG7769는 많은 관심을 끌고 있다.
노바티스의 경쟁 후보인 사바톨리맙은 골수이형성증후군 혹은 만성 골수단핵구백혈병-2 환자에서 2상, 3상 임상시험에 있다.
노바티스는 2상 연구 데이터를 보유하고 있고 2024년 3상 결과를 보고한 후, 승인을 신청할 계획이다.
로슈는 지난해 PD-1xTIM-3 이중특이를 2상 임상시험으로 이동했지만, GSK와 노바티스를 추격하고 있다.
릴리는 순수 항 Tim3 자산 LY3321367을 선호해, Tim3/PD-1 이중특이 항체인 LY3415233의 개발을 중단했다.
또한, BMS는 TIM-3 후보를 임상에 있지만 더 이상 활발한 임상 개발 프로그램 사이에 자산을 나열하지 않고 있다.
이밖에, 인사이트/아제누스, 시노, 아스트라제네카, 세르비에 등이 Tim3 후보들은 초기 임상에서 평가하고 있다.