그리폴스 독주 속 다케다‧CSL 등 신약 개발 경주
간에서 생성되는 보호 효소 억제제인 알파 1 항트립신(alpha 1 antitrypsin)이 부족한 유전 질환인 알파-1 항트립신 결핍증(AATD : alpha-1 antitrypsin deficiency)에 대해 일부 바이오파마 기업들이 개발을 위해 경주하고 있다.
AAT는 폐 손상을 보호한다.
오기능 유전자의 두 카피를 물려받은 AATD 환자들은 폐기종과 같은 폐질환에 걸릴 위험이 높다는 것을 의미한다.
간에서 종종 Z-AAT로 불리는, AAT의 변이되거나 잘못 겹친 버전이 축적되면서 점진적인 손상을 일으키고 드물게 간 이식이 필요한 경우가 있다.
AAT 증강 요법이 심각한 폐질환을 가진 사람들을 위해 개발됐지만 간 징후에 이용 가능한 특별한 치료법은 없다.
이런 치료는 주입을 위해 혈장에서 정상 AAT를 채취하는 것과 관련이 있지만, 이익은 오랫동안 논의되어 왔고 모든 국가에서 사용할 수 있는 것은 아니다.
AAT 증강 제품은 매우 비싸다는 것을 주목할 필요가 있다.
그리폴스(Grifols)는 10년 전 미국 바이오텍 탈레크리스(Talecris)와 함께 인수한 제품으로 지배적 입지를 구축하고 있다.
일본 다케다는 박스터를 통해 샤이어를 인수해 이 분야에서 진출했다.
다케다는 3억 달러의 선급금으로 작년 애로우헤드의 프로젝트에 대한 특정 권리를 취득해. 이 분야에 지속적인 관심을 높이고 있다.
파이프라인
리서치 업체인 EP(Evaluate Pharma)dp 따르면 주로 AATD에 의해 야기된 간 문제를 지향하지만, 파이프라인 측면에서 RNAi 접근법이 가장 앞서 있다.
애로우헤드의 ARO-AAT는 현재 진행 중인 2상 연구에서 올해 공개된 소규모 데이터를 기반으로 현재로서는 가장 유망한 것으로 여겨지고 있다.
TAK-999라 명명된 프로젝트는 간에서 변이된 Z-AAT 단백질의 생산을 차단함으로써 작동한다.
이 분야의 대부분의 연구처럼, 초점은 AATD의 심각한 합병증을 일으킬 가능성이 가장 높은 동형접합 PiZZ 변이를 가진 환자들에게 맞춰져 있다.
새로 공개된 AASLD 미팅 요약에서 24~48주간 전체 16명 환자의 2개 코호트에서 80~89%의 간에서 Z-AAT의 평균 감소율을 보였다.
간 기능과 섬유증 개선 징후도 보였다.
일부 애널리스트들은 ARO-AAT가 2022년에 미국에서 승인될 것으로 예상하고 있다.
더 엄격한 2상 Sequoia 임상은 등록이 완료됐고, 내년에 데이터를 생성하기 시작할 것으로 예측된다.
디세나(Dicerna)의 유사한 RNAi 치료제 벨세시란(belcesiran)이 추격하고 있지만, 지금까지 18명의 환자에 대한 초기 결과만 보고됐다.
이것은 유망했고, 더 대규모 2상 연구인 Estrella 임상은 이미 시작됐다.
알니람(Alnylam)이 미국 이외의 권리에 대해 옵션을 가지고 있지만, 벨세시란이 타케다와 애로우헤드에 대한 실제 경쟁자로 간주되려면 확실한 안전성이나 효능 이익을 보여야 한다.
다른 중간 단계의 경쟁자는 AATD 폐질환 환자를 목표로 하는 메레오(Mereo)이다.
회사의 프로젝트인 알벨레스타트(alvelestat)는 AAT에 의해 정상적으로 작용하는 역할인 폐 손상 호중구 엘라스타제(neutrophil elastase) 효소를 억제함으로써 작동되도록 제안되었다.
2상 임상은 주로 호중구 엘라스타제 활성의 바이오마커인 데스모신(desmosine)의 감소를 측정한다.
더 후기 파이프라인에는 AATD의 간과 폐 징후에 대한 해결책을 가지고 있다고 주장하는 인히브렉스(Inhibrx)와 센테사(Centessa)가 있다.
센테사는 분자 패치로 작용하는 ZF874를 연구하고 있다.
최근 3명 환자의 데이터를 통해 ZF874를 받은 환자 2명이 기능적 AAT 수준이 정상으로 회복됐다고 밝혔다.
그러나 한 환자의 독성 신호로 빛을 잃었다.
인히브렉스는 재조합 AAT-Fc 융합 단백질인 INBRX-101로 가장 간단한 접근방식을 추구한다.
회사 측에 따르면, 이는 AAT 증강 치료보다 더 편리하고 비용 효율적인 옵션을 제공할 수 있고 RNAi 접근법을 보완한다.
이밖에, CSL과 그리폴스(Grifols) 등이 일부 유전자 치료제를 전임상에서 평가하고 있다.
시장
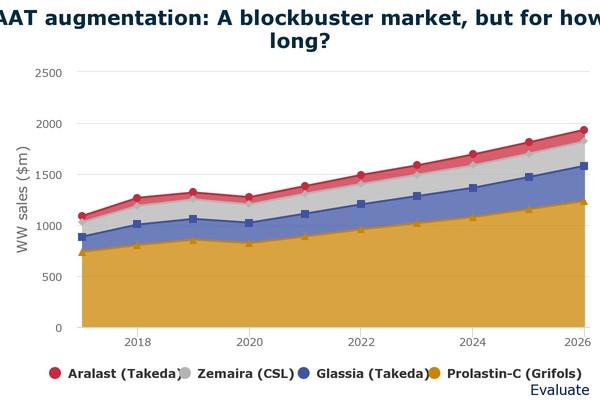
EP에 따르면, 현재 AATD 시장은 그리폴스의 프로라스틴-C(Prolastin-C)가 지배하고 있으며, 다케다의 아라라스트(Aralast), 글라시아(Glassia), CSL의 제마이라(Zemaira)가 추격하고 있다.
그리폴스의 프로라스틴-C 매출은 2020년 8.23억 달러, 2022년 9.57억 달러에서 2024년 10.78억 달러로 블록버스터에 도달하고, 2026년 12.36억 달러에 이를 전망이다.
다케다의 글라시아 매출은 2020년 2억 달러에서 2022년 2.46억 달러, 2026년 3.45억 달러 규모에 이를 것으로 추정된다.
아라라스트의 매출은 2021년 7500만 달러에서 2026년 1.15억 달러 규모로 예상된다.
CSL의 제마이라 매출은 2021년 1.96억 달러에서 2024년 2.19억 달러, 2026년 2.49억 달러로 추산된다.