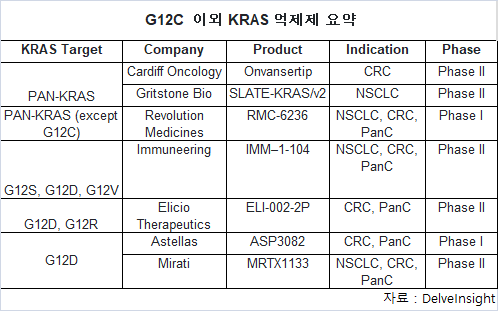
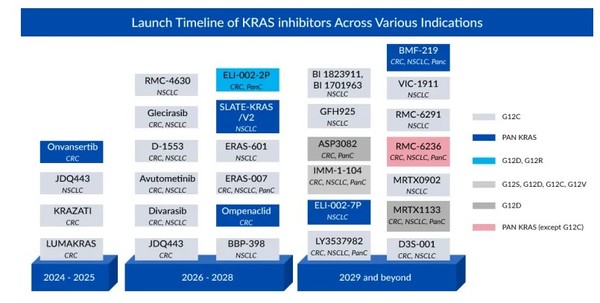
고형 종양 치료 유망한 발전‧빠른 진전 보여
암젠‧미하티 연구 주도…노바티스‧릴리‧로슈 등 개발 초기
KRAS 억제제의 출현은 무서운 고형 종양 퇴치에 희망을 주는, 빠르게 진전되는 종양 분야에서 주목할 만한 발전을 나타내며, 미래 종양 시장의 판도가 될 전망이다.
KRAS 변이 암에 대한 치료 환경은 최근 몇 년 동안 일부 유망한 발전과 함께, 빠르게 진전했다.
암 발병률 증가와 개인맞춤 암 치료에 대한 증가하는 수요에 힘입어, 향후 KRAS 억제제 시장은 상당한 성장이 예상된다.
진행 중인 연구와 임상 시험은 환자 결과 개선에 대한 긍정적 데이터로, 잠재적인 치료 전략을 계속 공유하고 있다.
컨설팅업체인 델베인사이트(DelveInsight)의 보고서를 보면 미국, 일본, 5EU 등 7대 주요 시장에서 KRAS 억제제 시장은 2032년까지 100억 달러 규모로 연평균 36% 고성장할 전망이다.
미국이 KRAS 억제제의 최대 시장으로, 7대 시장의 약 70% 시장 점유율을 차지할 것으로 예상된다.
미라티 테라퓨틱스, 노바티스, 암젠, 릴리, 베라스템(Verastem) 등 주요 업체들이 비소세포폐암, 대장암, 췌장암 등 다양한 적응증에 KRAS 변이에 대한 치료제 개발을 위해 경주하고 있다.
암젠과 미라티 테라퓨틱스(Mirati Therapeutics)는 암 치료에 대한 KRAS 억제제 개발 경쟁의 선두에 있다.
현재 두 회사의 후보들은 다른 KRAS 변이 해결에 상당한 격차를 남겨 둔, G12C 변이 종양 표적에만 초점을 맞추고 있다.
다른 변이에 대해 현재 승인된 치료제가 없기 때문에, 미충족 욕구가 높은 분야이다.
이런 문제를 인식한, 많은 주요 기업들은 적극적으로 대체 KRAS 변이체를 탐색하고 비소세포폐암을 넘어 다른 유형의 암까지 연구를 확대하고 있다.
이런 초점 변화는 더 광범위한 KRAS 변이를 해결하고 다수 암 유형을 표적으로 할 수 있는 효과적인 치료제 개발을 위한 유망한 잠재력을 가지고 있다.
카디프 온콜로지의 온반서팁(onvansertib), 그릿스톤 바이오의 SLATE KRAS), 후키파 파마의 HB-700) 등, 많은 기업들이 범 KRAS에서 후보 약물 개발에 집중하고 있다.
노바티스가 3상 임상 중인 JDQ443은 선택적, 공유 결합인 경구용 KRASG12C 억제제이다.
Ib상 KontRASt-01 연구의 초기 결과에서, 진행성 비소세포 폐암 환자에게 매일 2회 권장 용량 200mg은 57%의 전체 반응률(ORR)을 보였다.
현재, JDQ443은 순차적 또는 복합으로, 백금 기반 화학요법과 면역관문억제제 치료를 받은 KRASG12C 변이를 동반한 진행성 비소세포폐암 환자를 대상으로 도세탁셀에 대한 단독 요법으로 효과를 비교하는 3상 연구에 있다.
노바티스는 2024년까지 비소세포폐암에 대해 신약신청(NDA)을, 2026년 이후 대장암(CRC)에 대해 NDA를 제출할 계획이다.
베라스템 온콜로지의 아부토메티닙(Avutometinib, VS-6766)은 MEK와 ARAF, BRAF, CRAF와 관련된 비활성 복합체 형성을 촉발하는, RAF/MEK 집게로서 기능을 한다.
이 메커니즘은 더 지속된 효과를 유도하는, RAS 경로를 철저히 억제해 항종양 반응을 잠재적으로 높인다.
현재, 아부토메티닙은 개발의 진행 단계에 있다.
다른 MEK 억제제와 달리, MEK 키나제 활성을 차단할 뿐만 아니라 RAF가 MEK를 인산화하는 것을 방지한다.
이런 독특한 작용 방식은 아부토메티닙이 다른 억제제에서 관찰되는 한계인, 보정 활성화를 유발하지 않고 MEK 신호를 효과적으로 억제할 수 있게 한다.
FDA는 백금 기반 화학요법 등. 하나 이상의 이전 라인 치료 후, KRAS 상태에 관계없이, 재발성 저등급 장액성 난소암(LGSOC)이 있는 모든 환자 치료에 획기적인 치료제 지정을 해, FAK 억제제 데팍티닙(defactinib)과 복합으로 아뷰토메티닙의 잠재력을 인정했다.
RAMP 201 임상시험은 재발성 LGSOC 환자를 대상으로. 아뷰토메티닙 단독 또는 데팍티닙과 복합으로 등록을 목표로 하고 있다.
레볼루션 메디신(Revolution Medicines)은 SHP2의 기능을 명확히 방해하도록 설계된, 경구용 소분자 RMC-4630(SAR442720)을 2상 연구에 있다.
이런 필수 세포 단백질은 수용체 티로신 키나제부터 RAS까지 신호를 전송하여 세포 생존과 증식을 조절한다.
현재, 회사는 KRAS G12C 변이가 있는 비소세포폐암 환자를 대상으로 RMC-4630과 소토라십(sotorasib)의 복합을 평가하고 있다.
베링거 인겔하임은 주요 G12 및 G13 온코단백질을 표적으로 하는, 다양한 종양 발생 변이에 걸쳐 KRAS의 활성을 억제하하는 BI 1701963을 초기 단계 연구에서 평가하고 있다,
메커니즘은 KRAS를 활성화에 중요한 구성 요소인 SOS1에 결합과 관련이 있다.
전임상 연구는 단백질에서 흔히 관찰되는 많이 테스트된 G12 및 G13 KRAS 변이에서 종양 성장을 방해하는 이 범-KRAS 억제제의 효과를 입증하고 있다.
현재 1상 시험이 진행 중인 BI 1701963은 KRAS 변이를 수반한, 진행성 또는 전이성 고형 종양 환자에 대한 단독요법과 트라메티닙(trametinib)과 복합 모두에서 평가하고 있다
베링거는 루마크라스(LUMAKRAS)와 복합으로 BI 1701963의 잠재력을 탐색하기 위해 암젠과 임상 협력을 시작했다.
로슈의 경구용 소분자인 디바라십(Divarasib/GDC-6036)은 전임상 시험에서 KRAS G12C 단백질의 강력하고 특이적 억제를 보였다.
AACR에 2023에서 발표된 Ib상 연구 결과를 보며느 GDC-6036과 세툭시맙(cetuximab)의 복합은 주목할 임상 효능과 우수한 안전성 수준을 보이는 등, 대장암 치료에 효과를 확인했다.
로슈의 LY353798은 예비 연구에서 단독과 다른 항암제와 복합 모두 효능을 보인, KRAS G12C의 특정 공유 결합 차단제이다.
현재 비소세포폐암, 대장암 또는 다른 진행성 고형 종양 환자를 대상으로 1상 임상에 있다.