애브비 ‘휴미라’ 유일하게 승인…10여개 업체 개발 경주
UBS‧인사이트‧아셀리린, 일부 긍정적 업데이터 결과 공유
자가면역 블록버스터의 범위를 확대하기 위한 새로운 기회를 위해, 많은 바이오파마 기업들이 피부병 화농땀샘염(hidradenitis suppurativa)에 초점을 맞추고 있다.
현재 화농땀샘염의 유일한 치료제는 올해 미국 특허가 만료된 애브비의 휴미라(Humira)이기 때문에, 경쟁자들은 휴미라와 바이오시밀러 버전보다 유리한 프로파일이 필요할 수 있다.
최근 AAD(American Academy of Dermatology) 연례미팅에서 UCB의 빔젤스(Bimzelx), 아셀리린(Acelyrin)의 이조키벱(izokibep)에 대해 각각 3상 연구 결과를 공유했다.
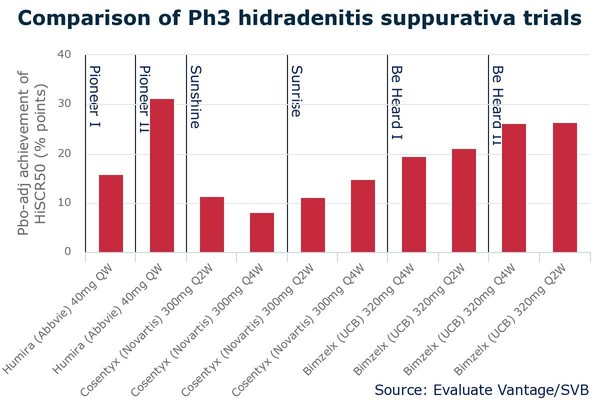
중등도에서 중증의 화농땀샘염(HS) 환자 각각 500명 이상이 등록된, UCB의 Be Hear I와 Be Hear II 임상시험은 위약군에 대해 항IL-17A/17F 항체인 빔젤스를 2주와 4주마다 투여했다.
주요 최종목표는 4개월 치료 후, 농양이나 배수 터널 수의 증가 없이, 총 농양과 염증성 결절 수에서 최소 50% 감소로 정의된, HiSCR50(hidradenitis suppurativa clinical response 50)의 달성이었다.
UCB는 두 연구의 데이터가 통계적으로 유의하고 임상적 유의한 개선을 보였으나, 실제로 Be Hear I에서 월간 투여는 유의하지 않았다고 밝혔다.
또한, 2차 최좀목표인 16주차에서 더 엄격한 측정 HiSCR75에 대해 개선을 보였으나, Be Hear I에서 더 적은 빈도 투여는 유의함을 보이지 못했다.
노바티스는 올해 미국과 유럽연합(EU)에서 HS에 코센틱스(Cosentyx)의 승인을 예상하고 있다.
리서치 업체인 EP(Evaluate Pharma)의 보고서를 보면 교차 임상기준으로, 빔젤스는 코센틱스보다 더 나은 반응을 보였지만, UCB 프로젝트는 Pioneer II 임상에서 보여준 데이터가 휴미라의 데이터보다 약간 뒤처져 있다.
UCB의 주장은 안전성이 될 수 있다.
빔젤스의 가장 일반적인 부작용은 땀샘연, 구강 칸디다증, 두통, 설사인 반면, 휴미라의 라벨에는 심각한 감염, 악성 종양에 대해 박스 경고가 표시되어 있다.
UCB는 하반기에 중등도에서 중증 HS에 대해 빔벨스의 승인을 신청할 계획이다.
아셀리린의 이중특이 나노바디 이조키벱에 대한 데이터도 고무적이었다.
이번 업데이트는 이미 유망함을 보여준, 2b/3상 HS 연구의 A부분에서 나왔다.
3개월간의 치료 후, 전체 질병의 제거를 지속하는, HiSCR50, HiSCR75, HiSCR90, HiSCR100은 파트 A에서 각각 환자의 71%, 57%, 38%, 33%까지 도달했다.
하지만 위약 그룹 없이, 이러한 데이터를 다른 최종단계 프로젝트와 비교하기 어렵고, 파트 A는 30명의 환자만 포함했다.
이조키벱은 칸디다 감염없이, 우수한 내성을 보였고, 주사 부위 반응은 환자의 40%에서 관찰됐다고 회사는 밝혔다.
아셀리린은 이 데이터를 바탕으로 HS에 두 번째 3상 시험을 시작할 계획이다.
인사이트는 성인 HS 환자를 대상으로 경구용 JAK1 억제제인 포보르시티닙(povorcitinib, 이전 INCB54707)에 대한 2상 임상시험에서 새로운 52주 데이터를 보고했다.
2상 연구는 포보르시티닙의 안전성과 효과성을 평가하기 위해 설계되었다.
연구 결과에 따르면, 하루 한 번 포보르시티닙 75mg로 장기 치료는 모든 치료 그룹에 걸쳐 지속적인 효능을 보였다.
연구는 포보르시티닙 75mg를 받은 모든 참가자가 이 용량으로 전환한 후 모든 치료 그룹에 대해 지속적인 효과를 입증한 36주 기간이 포함된다.
52주에서, 경구 억제제는 높은 임계값 결과에서 지속적인 효과를 보였다.
또한, 일반적으로 우수한 내약성을 확인했고 이전 데이터와 일치하는 안전성 프로파일을 보여주었다.
회사는 중등도에서 중증 HS 환자를 대상으로 진행 중인 3상 연구를 통해 포보르시티닙의 개발을 계속 진행할 예정이다.
이밖에, 화이자, J&J, 릴리, 애브비, 암젠 등 빅 파마를 비롯해, 인플라알엑스(InflaRx), 체모센트릭스(ChemoCentryx), CSL 베링, 키메라 테라퓨틱스(Kymera Therapeutics), 아클라리스테파퓨틱스(Aclaris Therapeutics), 베링거인겔하임, 아조라 테라퓨틱스(Azora Therapeutics) 등 향후 HS 치료에 이용할 수 있는 새로운 약품을 개발하고 있다.
컨설팅업체인 DBR(DelveInsight Business Research)의 최신 보고서를 보면, 미국, 일본, 5EU 등 7대 제약시장에서 HS 치료제 시장은 2021년 약 11.5억 달러를 기록했고 2032년까지 연평균 10.2% 성장할 전망이다.
EP는 HS가 건선처럼 붐비는 시장이 되기까지는 시간이 걸릴 것이지만, 12개 이상의 후보들이 2상 임상시험에서 평가되고 있다고 밝혔다.