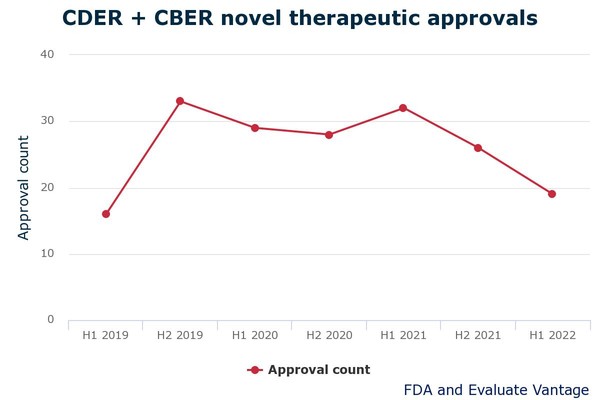
1H 19개 허가, 2H 22개 예상, 10년간 평균 이하
릴리 항당뇨병제 ‘모운자로’ 2028년 매출 74억$로 최대 승인

FDA의 신약 승인 둔화는 바이오파마를 초조하게 하고 있다.
그 부문이 약세 시장을 물리치기 위해 고군분투하고 있는 상황에서, 억제된 개발자들이 마지막으로 필요로 하는 것은 규제 걱정이다.
FDA CDER와 CBER 부서는 올해 상반기 19개 신약에 대해 청신호를 보냈지만, 이는 2019년 이후 최저 6개월 수치이다.
리서치 업체인 EP(Evaluate Pharma)에 따르면, 이런 침체는 FDA 직원 부족에서부터 아두헬름(Aduhelm) 이후 기준 강화와 새로운 FDA 국장의 선임 등까지 다양하다.
EP는 올해 하반기 22개 신약이 승인을 기다리고 있어, 이들 모두가 예상대로 청신호를 받을 경우, 올해 승인된 약품은 41개에 이를 것으로 추정했다.
이는 지난 5년간에 비해 침체이고, 또한 10년 평균인 48개에도 미치지 못한다.
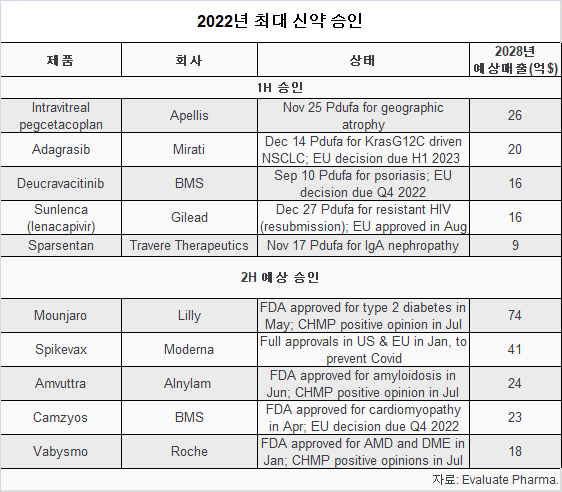
승인 약품 5년 후 매출 전망
EP가 추정한 올해 승인된 약품의 5년 후(2028년) 예상 매출 톱10 중 6개가 승인됐다.
이미 승인된 약품 중, 릴리의 2형 당뇨병 치료제 모운자로(Mounjaro)가 2028년 예상 매출 74억 달러로 1위를 차지했다.
모더나의 코로나19 백신 스파이크백스(Spikevax)의 예상매출은 41억 달러로 2위에 랭크됐다.
알닐람의 아밀로이드증 치료제 암부트라(Amvuttra)와 BMS의 심근증 약품 캄지오스(Camzyos)가 각각 24억 달러, 23억 달러의 5년 후 매출이 예상된다.
로슈의 연령관련 황반변성 치료제 바비스모(Vabysmo)는 2028년 18억 달러, 길리어드 사이언스의 내성 HIV 약품 선렌카(Sunlenca, lenacapivir)는 16억 달러의 매출이 예상된다.
선렌카는 8월에 EU에서 승인됐지만, 미국에서 12월 28일에 최종 결정일이 예정돼 있다.
올해 하반기는 BMS, 아펠리스 등에게 큰 결정이 남아 있다.
11월에는, 블록버스터 매출이 예상되는, 아펠리스의 페그세타코플란(pegcetacoplan)과 트라베어(Travere)의 스파르센탄(sparsentan)을 포함해, 7개 약품이 FDA 최종결정(Pdufa)을 기다리고 있다.
유니큐어와 파트너 CSL의 혈우병 B에 대한 첫 유전자 치료제도 11월에 승인될 수 있다.
12월은 미라티(Mirati)의 아다그라십(adagrasib)과 TG 테라퓨틱스의 유블리툭시맙(ublituximab)에 대한 결정이 대기 중이다.
연말까지, 항PD-1/L1 공간에서, 노바티스/베이젠의 티슬렐리주맙(tislelizumab)과 코헤루스/상하이 준시의 토리팔리맙(toripalimab)이 미국 시장 진출을 기대하고 있다.
하반기 승인 예상 약품 중, 페그세타코플란, 듀크라바시티닙(deucravacitinib)과 선렌카가 가장 주목을 받고 있다.
아펠리스의 지도모양 위축에 대한 유리체 내 페그세타코플란은 2026년 예상 매출 26억 달러로 하반기 승인 약품 중 톱이다.
2028년 예상 매출을 보면, 미라티의 폐암 약품 아다그라십은 20억 달러, BMS의 건선 치료제 듀크라바시티닙와 선렌카는 각각 16억 달러이다.
트라베어의 IgA 신증 치료제 스파르센탄은 9억 달러의 매출을 예상된다.
EP는 TG의 우블리툭시맙, 프로벤션 바이오의 PRV-031, 미라티의 아다그라시브에 대해 의문이 있다고 지적했다.