릴리의 항당뇨병제 ‘모운자로’ 등 4개 신약 블록버스터 예상
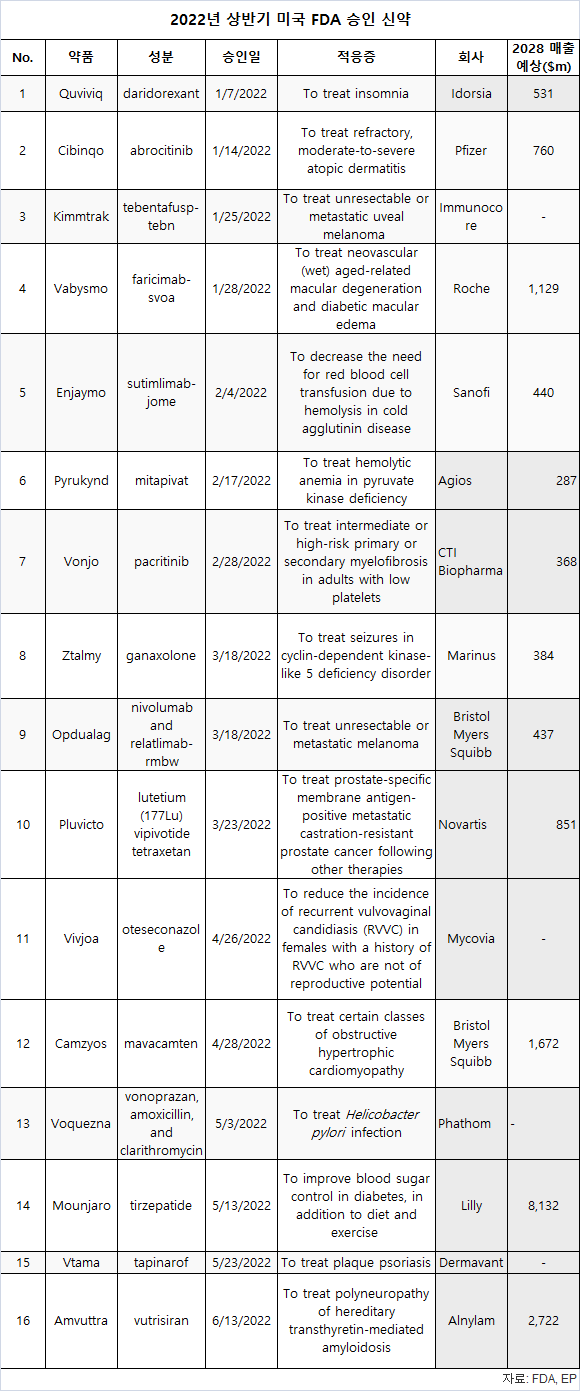
올해 상반기, 미국 FDA는 16개 신약과 6개 바이오로직(BLA)을 승인했다.
또한 일부 약품은 적응증 확대 승인을 받은 반면, 일부는 다양한 질병의 치료에 게임체인저가 될 것으로 예상된다.
생명과학 정보제공 업체인 EP(Evaluate Pharma)에 따르면, 16개 신약 중, 릴리의 모운자로(Mounjaro, tirzepatide) 등 4개 약품이 2028년까지 연간 10억 달러 이상의 블록버스터 매출을 달성할 것으로 예상된다.
2형 당뇨병 치료에 승인된, 모운자로는 다른 항당뇨병제와 비교해 효과를 입증했을 뿐만 아니라 15~23 파운드의 체중 감량을 입증했다.
EP는 모운자로의 매출은 2028년까지 81억 달러 이상에 이를 것으로 추정하고 있다.
알닐람의 유전성 트랜스티레틴 매개 아밀로이드증의 다발 신경병증 치료제인 암부트라(Amvuttra, vutrisiran)는 2028년 27억 달러 이상의 매출이 예상된다.
또한, BMS의 폐쇄성 비대 심근증 치료제 캄지오스(Camzyos, mavacamten)와 로슈의 습성 나이관련 황반변성과 당뇨병성 황반부종 치료제인 바비스모(Vabysmo, faricimab-svoa)는 각각 2028년 16.7억 달러, 11.3억 달러의 매출에 이를 전망이다.
상반기에 다른 주요 승인은 노바티스의 전립선암 치료제 플루빅토(Pluvicto, lutetium (177Lu) vipivotide tetraxetan)와 화이자의 아토피 피부염 치료제 시빈코(Cibinqo, abrocitinib), 이도르시아의 불면증 약품 큐비빅(Quviviq, daridorexant) 등이 있다.
이런 약품의 2028년 매출은 각각 8.5억 달러, 7.6억 달러, 5.3억 달러에 이를 것으로 EP는 추장하고 있다.
다른 획기적인 신약은 마리누스 파마슈티컬스(Marinus Pharmaceuticals)의 뇌전증의 희귀 형태인 사이클린 의존성 인산화효소 유사 5 결핍장애(CDD)와 관련된 발작을 경험하는 환자의 치료에 승인된 지탈미(Ztalmy, ganaxolone)이다.
지탈미는 이런 CDKL5 결핍 장애에 대해 특별히 승인된 첫 약품이다.
올해 하반기, 환자에게 게임 체인저가 될 가능성이 높고 개발 회사들의 주요 자산이 될, FDA 승인을 기다리는 많은 신약이 있다.
올해 하반기 승인을 기다리고 있는 약품들 중에는 근위축성 측삭경화증(ALS) 치료제, 초기 활동성 뇌부신백질형성장애로 진단된 소아 환자에 대한 유전자 치료제 등이 있다.
아미릭스 파마슈티컬스(Amylix Pharmacuticals)는 이미 캐나다에서 승인된, ALS 치료제 AMX0035(Albrioza)의 승인을 기대하고 있다.
알브리오자라는 상표명으로 시판될 AMX0035의 승인은 2018년 이후 국내에서 승인된 첫 ALS 신약이다.
블루버드 바이오(bluebird bio)는 베타지중해빈혈과 경상적혈구 질환에 대한 2개의 유전자 치료제의 승인을 기다리고 있다.
노바티스와 BMS가 각각 개발한 항암제인 티슬리주맙(Tislelizumab)과 데우크라시티닙(Deucravacitinib)도 승인을 기다리고 있다.
다수의 신약들이 승인을 기다리고 있지만, FDA가 지난 2년 동안 기록한 추세를 유지하려면 신약에 대한 청신호의 속도를 높일 필요가 있다.
FDA는 2021년 50개, 2020년 53개의 신약을 승인했다.
한편, FDA는 J&J의 다발성 골수종 치료제 카빅티(CARVYKTI, ciltacabtagene autoleucel) 등 6개 바이오로직 신청을 허가했다.