작년 22개 허가…바이오로직 절반 이상 차지
2016년 신약 승인에서 실망스런 한해였다.
미국 FDA는 2015년 45개 신약으로 최대 승인을 기록한 후 작년 22개로 2010년 이후 최저를 기록했다.제약산업의 R&D 생산성이 낮을수록 적절하게 구입할 수 있는 약물은 더 멀어진다.
FDA는 신약 승인은 감소한 것이 아니라 신청을 하지 않은 약물을 승인할 수 없다는 입장이다.2016년 예상된 5개를 신속 승인했다고 지적했다.
약물 R&D 평가에 사용되는 많은 지표들이 의미있게 변하지 않았다.현재 1540억 달러 R&D 지출은 성장을 유지했지만 신약 승인 수는 줄어들었다.
13개 빅 파마는 2015년 41%에 비해 2016년 36% 신약 승인을 받았다.2년간 41% 신약이 새로운 활성 방법을 표적으로 1차 라인으로 승인됐다.
암, 감염, 혈액질환, 중추신경시스템이 2016년 73%, 2015년 71%로 선두 치료 분야였다.바이오로직 약물들은 55%(2015년 39%)로 처음으로 다수 승인을 받았다.
더 높은 비율은 시장에 신속하게 진출하는 FDA 프로그램의 덕을 봤다.최근 수년간 실적이 우수했던 GSK, 노바티스, J&J는 2016년에 신약을 승인받지 못했다.
암젠, 아스트라제네카, 바이엘, BMS 등도 작년 승인된 신약이 없었다.2015년 14개 신약을 승인받은 13개 빅 파마 중 7곳은 2016년은 빈손이었다.
나머지 6개 기업들은 6~8개로 증가를 보였다.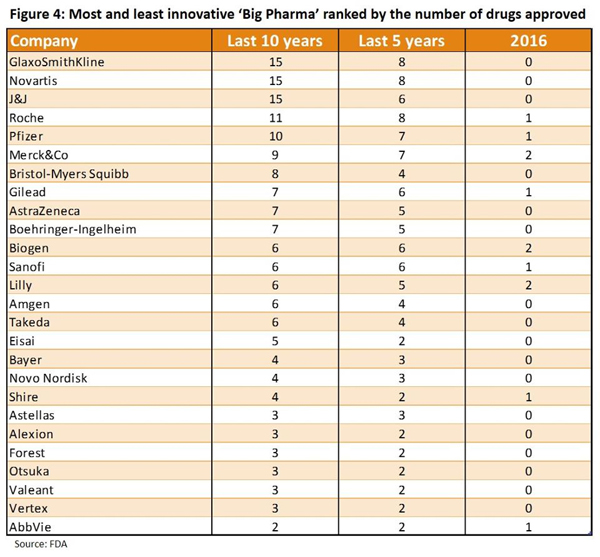
애널리스트들은 기업들은 과정 개선, 재편, 조직화에 지속적인 초점을 맞춰야 한다고 조언하고 있다.
일부 기업들은 R&D 운영을 개편하고 있다.J&J, GSK, 노바티스 등 일부는 확실한 성공이 있는 과도한 혁신을 추진하고 있다.
BMS, 베링거인겔하임, 바이오젠, 노보노디스크, 길리어드 사이언스 등은 더 적은 구조 비용을 기능적으로 특수 바이오파마 모델을 지지하고 있다.경제적 약물 R&D로 변모할 최대 기회는 가장 비싼 장애인 경제적 데이터의 수집으로 변화에 달려있다.
새로운 데이터 수집 기술들이 급격히 출현하고 있다.일반적 사업은 제약산업에 실제 위협이 된다.
변화하는 경제적 약물 R&D에서 성공 부족은 결과에도 불구하고 포퓰리즘 정책의 손상을 필연적으로 유도할 것이다.현재 약물 특허 만료는 복잡하고 불투명하다.
빅 파마는 다양한 전략을 통해 특허를 더 확대하고 있다.이는 약물의 라이프사이클 관리의 중요한 일부이다.
더 긴 특허수명을 달성하는 많은 방법들이 있다.새로운 특허는 제조과정부터 신약 제형까지 어떤 것이든 취득할 수 있다.
IMS에 따르면 모든 상업적으로 중요한 약물의 42%가 미국 특허를 연장했다.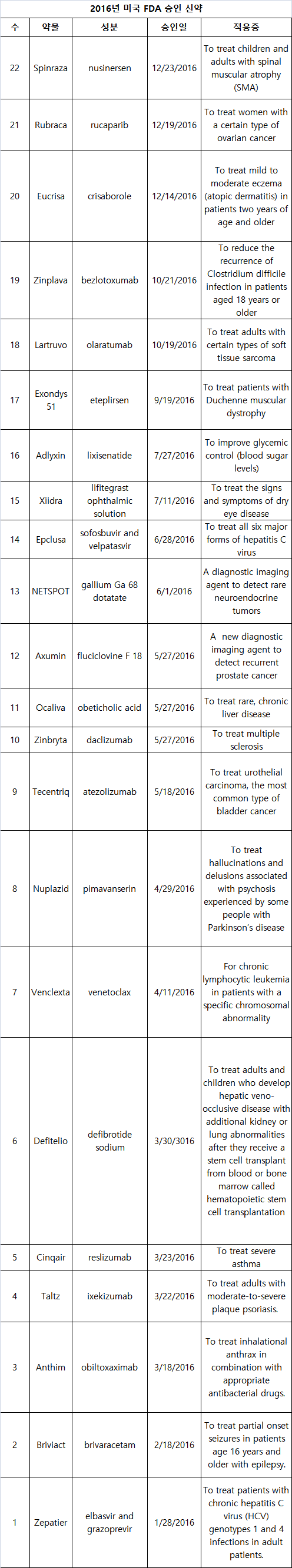
고재구 기자
news@pharmstoday.com

