1상 및 3상 각각 44건 승인…연구자 임상 28건
올해 1분기 신약개발을 위한 임상시험 142건이 승인된 가운데 서울대병원이 9건으로 가장 많은 것으로 분석됐다.
식품의약품아전처의 '임상시험 승인현황'에 따르면, 1분기 142건의 임상시험이 승인됐다. 지난해 1분기 146건과 비슷한 수치다.
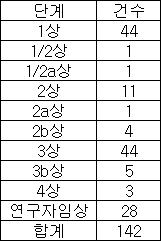
임상시험 단계별로 보면 임상3상과 임상1상이 각각 44건으로 가장 많았으며, 연구자임상 28건, 2상 11건 등이다.[도표 참고]
제3상 임상시험의 경우 국내 제약사보다는 다국적 제약사가 다수를 차지했다. 반면 제1상 임상시험이 경우 다국적 제약사보다는 국내 제약사가 주를 이뤘다.
다국적 제약사들이 아직도 초기 임상시험에 해당하는 제1상 임상시험보다는 시판허가를 받기 위한 임상3상시험에 주력하고 있다는 것으로 풀이된다.
국내 제약사의 경우 일부 제약사를 제외하고 신약개발 등을 위한 임상시험을 시작한지 얼마되지 않아 초기 임상시험 비중이 높기 때문에 이같은 결과를 보이고 있다는 설명이다.
제2상 임상시험 11건이 경우 제넥신과 서울대병원 내과, 한미약품 등에서 승인을 받은 4건을 제외하고 나머지는 다국적 제약사에서 승인을 받은 것이다.신청기관별로 보면 서울대병원이 9건으로 가장 많았다. 서울대병원은 9건 중 8건이 연구자임상시험이며, 서울대병원 내과에서 승인을 받은 '보트리엔트'를 이용한 임상시험은 제2상 임상시험이다.
그 다음으로 한국노바티스와 일동제약이 각각 6건, 한미약품과 한국화이자제약이 각각 5건 등의 순이었다.후기 임상시험에 해당하는 제4상 임상시험도 3건이 승인을 받았다.
임중선 기자
alrhr@pharmstoday.com

