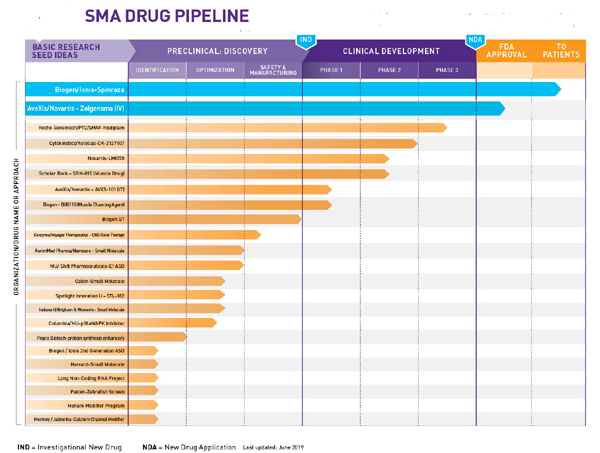
로슈, ‘리스디플람’ 연말 승인 신청 예상…‘스핀라자’ ‘졸젠스마’와 경쟁
바이오젠의 SMA 치료제 스핀라자(Spinraza)는 노바티스의 최근 승인된 유전자 치료제 졸젠스마(Zolgensma)로부터 주요 위협에 직면해 있고 영토를 지키고 매출 성장을 유지에 도움이 되는 강력한 데이터가 필요하다.
최근 로슈는 개발 중인 SMA약품 리스디플람(risdiplam)의 톱라인 임상 3상 연구 데이터를 발표했다.리스디플람은 SMA 환자의 운동 기능을 개선할 수 있음 보인 임상 3상 데이터로 로슈는 SMA 시장의 일부를 점유할 수 있다는 기대에 부풀어 있다.
SUNFISH 연구 결과에서 리스디플람으로 치료 1년 후, 2~25세 2형 혹은 3형 SMA 환자는 위약군과 비교해 MFM-32(Motor Function Measure 32) 척도에 대해 더 우수한 점수를 가진 것으로 나타났다.데이터는 올 연말 전에 미국과 다른 시장에서 리스디플람의 승인 신청을 지지할 수 있다고 로슈가 밝혔다.
로슈는 2020년 승인을 기대하고 있다.청신호를 받을 경우, 리스디플람은 바이오젠의 블록버스터 안티센스 기반 SMA 약품 스핀라자(nusinersen)는 물론 노바티스의 졸젠스마(onasemnogene abeparvovec)와 시장에서 경쟁하게 된다.
스핀라자와 졸젠스마 모두는 가격이 비싸다.스핀라자는 미국 도매가로 첫해 75만 달러, 이후 37만 5000달러인 반면, 졸젠스마의 1회 가격은 210만 달러이다.
스핀라자는 2017년 승인돼 시장에서 더 확고한 입지를 구축하고 있고 올해 9개월간 매출은 15.5억 달러로 전년동기대비 23.9% 급증했다.스핀라자의 올 3분기 매출은 5.5억 달러로 연간 17% 신장했다.
미국 매출은 5.7% 증가한 2.4억 달러, 미국 이외는 3.1억 달러로 27.3% 증가했다.바이오젠의 분기 보고서를 보면, 스핀라자의 환자 수는 2분기 말과 비교해 3분기에 미국에서 3%, 미국 이외에서 18% 증가했다.
스핀라자의 3분기 매출은 약간 둔화를 보였지만, 회사는 노바티스의 약품과 경쟁으로 하락이 아니라고 주장하고 있다.졸젠스마는 SMA 시장의 5% 정도를 차지하는 2세 미만 모든 유형 SMA 어린이에게만 승인됐다.
졸젠스마의 첫 전체 분기 실적인 3분기 매출은 1.6억 달러를 기록했다.졸젠스마의 한 가지 이슈는 나이와 함께 더 일반적이 되는 약품을 전달하는 데 사용된 바이러스에 노출된 환자들에게 효과가 적다는 것이다.
파트너인 PTC 테라퓨틱스와 공동으로 개발 중인 리스디플람은 표적 나이 범위 측면에서 스핀라자에 더 근접한 경쟁자이고 경구 약품이라는 한 가지 장점이 있는 반면, 스핀라자는 척추 강내에 주사해야 한다.다른 면에서, 리스디플람은 매일 복용해야 하는 반면 스핀라자는 첫 추가 기간에 수해 주사 후 4개월마다 투여한다.
로슈는 리스디플람 임상에서 지금까지 중도 연구 탈락을 유도하는 안전성 문제는 없었다고 약품의 안전성을 강조하고 있다.최근 SMA 2형 환자에 대한 척추 강내 주사 경로와 관련된 졸젠스마의 한 연구는 동물 연구에서 약품의 위험 가능성을 지적한 후 중단됐다.
월가의 애널리스트들은 졸젠스마는 새로 진단된 환자, 스핀라자와 리스디플람은 질병이 더 진행된 나이 많은 환자에게 사용으로 3개 약품은 시장을 3등분할 것으로 예상했다.SMA 시장에서 경쟁은 로슈의 리스디플람의 예상된 향후 승인으로 더 치열해질 전망이다.