유전자 치료제 등 개발 경주…‘헴리브라’ 추격
미국 FDA는 작년 말 유전 실명의 한 유형의 치료에 첫 유전자 치료제를 승인했다.
혈우병 등 치료에 많은 다른 유망한 치료제들이 시장에 빠르게 출시되고 있다.혈우병은 스파크 테라퓨틱스, 바이오마린 파마슈티컬, 유니큐어 등 많은 유전자 치료제 중심 제약사를 이미 유혹하고 있다.
이것은 주로 출혈 예방과 치료를 위해 환자들이 복용하는 약품들이 연간 50만 달러를 넘을 수 있는 가격과 때때로 일주일에 여러 번 약을 주입해야 하기 때문이다.관련 업계에 따르면 현재 연간 100억 달러 규모로 추정되는 혈우병 시장에서 유전자 치료를 첫 번째 승인은 강력한 상업적 기회와 기존의 전략적 장점이 있다.
혈우병 약품을 마케팅하는 제약사들은 유전자 치료제의 도래로 압박을 받을 것이다.유전자 치료 위협은 앞으로 더 커질 것이고 시간이 지남에 따라, 이런 치료법은 더 안전하고, 더 효과적이며, 더 광범위하게 적용될 것으로 예상된다.
상가모 테라퓨틱스(Sangamo Therapeutics), 크리스퍼 테라퓨틱스(Crispr Therapeutics) 등 기업들이 테스트하고 있는 유전자 퍈집 기술은 이런 과정을 더 가속화할 수 있다.새로운 연구
투자 리서치 회사인 AllianceBernstein에 따르면 미국 혈우병 시장은 46억 달러 규모로 예측된다.
이들은 매우 비싼 바이오로직이다.
혈우병 시장의 특징 중 하나는 매우 경쟁적이지만 가격이 떨어지지 않는다는 점이다.인간 혈장에서 추출한 첫 혈우병 치료제는 1960년대 중반에 출시됐다.
하지만 1980년대에 HIV가 출현했을 때, 불행히도 이런 제품들은 약 4000명의 혈우병 환자들이 감염된 혈액 공급으로 HIV를 퍼트렸다.1990년대에 제조가 어려운 재조합 DNA 기술을 사용한 동물 세포에서 인간의 응고 단백질을 복제한 것이 바통을 이어 받았다.
바이엘은 코제나이트(Kogenate)를 판매했다.치료제들이 개선되고 있는 곳에 기술이 발전하고 있다.
로슈는 차세대 혈우병 A 치료제 헴리브라(Hemlibra)로 가장 앞서 있지만 알리람/사노피의 피투시란(fitusiran)과 스파크 테라퓨틱스와 바이오마린의 유전자 치료제들 등 다른 새로운 프로젝트들이 뒤를 잇고 있다.사노피는 알니람으로부터 RNAi 제품 피투시란을 라이선스했다.
바이오마린의 유전자 치료제 valoctocogene roxaparvovec(BMN 270)은 WFH(World Federation of Hemophilia) 미팅에서 임상 I/II 201 연구에서 업데이트된 데이트를 공개했다.지난 5월 바이오마린은 심각한 혈우병 A에 유전자 치료제인 valoctocogene roxaparvovec의 업데이트된 임상 I/II 데이터를 발표했다.
회사는 심각한 혈우병 A의 포괄적 유전자 치료에 대한 6건 임상을 진행하고 있다.심각한 혈우병 환자의 혈청학을 평가하는 2개 임상3상, 1개 임상 I/II, 2개 추가와 별도 연구와 혈우병 A 환자의 기본 특성을 평가하는 하나의 비 중재 연구 등이다.
같은 달 스파크와 파트너인 화이자는 혈우병 B에 대한 SPK-9001의 임상 I/II 데이터를 공개했다.모두 15명 참가자는 팩터 IX의 정기 주입을 중단했다고 보고했다.
장기 지속 팩터 VIII 분야에서도 여전히 활동하고 있다.미팅에서 기존 확대 반감기 제품에 대한 1주에 2번과 비교해 예방으로 1주 한번 이하로 투여하도록 디자인된 현재 사노피가 인수한 바이오베라티브의 BIVV001에 대한 첫 인간 데이터가 주목을 받았다.
피하주사제인 헴리브라는 1주일 1회 투여제제로 승인됐다.임상 I/II Exten-A에서 저용량 BIVV001은 37시간 반감기를 보인 반면 표준 제조합 FVIII 치료제는 13시간이었다.
유니큐어는 혈우병 B 유전자 치료제 AMT-061의 초기 임상 데이터를 최근 발표했다.
3명의 혈우병 B 환자를 대상으로 AMT-061 1회 용량을 투여 6주 후 환자의 31%가 팩터 IX 활동이 정상인 것으로 보고했다.
회사는 미국과 유럽 당국에 이런 임상 2b 데이터를 올해 제출할 예정이다.
FDA는 바이오마린과 스파크 프로젝트 등 아데노 관련 바이러스(AAV ) 벡터를 사용하여 유전자 치료에 대한 추적 조사를 최소한 5년 이상 요구할 것이라고 밝혔다.
경쟁
6월 FDA는 팩터 VIII 억제제없이 혈우병 A 환자에 대해 헴리브라의 적응증 추가 신청을 수용, 10월 승인했다.
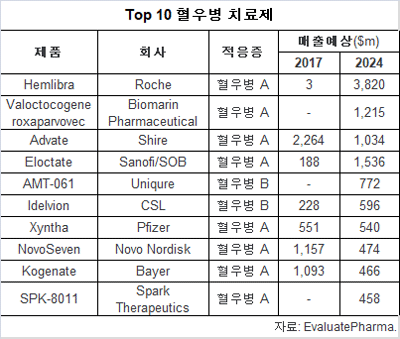
EP는 2024년 톱10 혈우병 치료제로 항 팩터 IXa & X 이중특이 단클론항체인 헴리브라(38억$), 사노피/SOB(Swedish Orphan Biovitrum)의 엘록태이트(15.36억$), 바이오마린의 유전자 치료제 Valoctocogene roxaparvovec(12억$), 애트바트(10.3억$), 유니큐어의 혈우병 B 유전자 치료제 AMT-061(7.7억$) 등을 예상했다.
현재 리더인 애드바트의 매출은 2017년 22.6억 달러를 기록했고 노보세븐은 11.5억 달러, 코제네이트는 10.9억 달러를 올렸다.시장에 이미 이런 초대형 제품들이 있어 새로운 약품들은 억제제 그룹이나 매우 더 큰 비억제제 환자에 대해 헴리브라의 효능에 필적해야 할 것이다.

