식약처, 안전성 서한 배포…미 FDA, 메트헤모글로빈혈증 유발 경고
24개월 미만 영아에게 사용되는 벤조카인 함유 제제가 메트헤모글로빈혈증을 유발할 수 있다는 경고에 따라 미국에서 판매 중지됐다.
식품의약품안전처는 구강 국소마취 등에 사용하는 벤조카인 함유 제제에 대해 24개월 미만 영아에게 사용을 금지하는 내용을 담은 안전성 서한을 배포했다.이번 조치는 24개월 미만의 영아에게 해당 제품 사용 시 혈액을 통해 운반되는 산소의 양이 현저히 줄어드는 '메트헤모글로빈혈증(methemoglbinemia)'유발할 수 있다는 미국 FDA의 경고에 따른 것이다.
FDA는 24개월 미만 영아에게 사용하는 벤조카인 함유 제품의 시판을 중지하고, 지난 24일 24개월 이상의 어린이 및 성인에게 사용하는 제품 표시(라벨)에 변경하도록 조치했다.제품 표시 사항에는 메트헤모글로빈혈증에 대한 경고 문구 추가와 함께 24개월 미만 영아에게 사용 금지, 부모 및 보호자가 24개월 미만 영아에게 사용하지 않도록 했다.
식약처는 이번 안전성 서한을 통해 의사 등 전문가에게 동 제제 처방·조제 시 환자에게 메트헤모글빈혈증의 위험성과 그 증상에 대해 알리고 천식, 폐기종 환자, 고령자 등 고위험군에게는 신중하게 사용해 줄 것을 당부했다.또 환자에게는 창백함, 회색이나 푸른색을 띠는 피부, 숨가뿜 등과 같은 메트헤모글로빈혈증 증상이 나타날 경우 즉시 의약전문가와 상의할 것을 권고했다.
식약처는 해당 제제의 허가사항에 ‘메트헤모글로빈혈증’이 유발될 수 있음을 인지할 수 있도록 경고 문구를 강화하고, 24개월 미만 영아에게 사용금지하도록 하는 등 안전성 강화조치를 취하기로 했다.
현재 국내에 허가된 벤조카인 함유 구강용 제품은 태극제약의 ‘이클린케어겔20%’ 등 9개사 15품목(수출용 5개 포함)이며, 2016년 생산·수입실적은 약 10억 9000만원(수출용 약 6억 4000만원 포함)이다.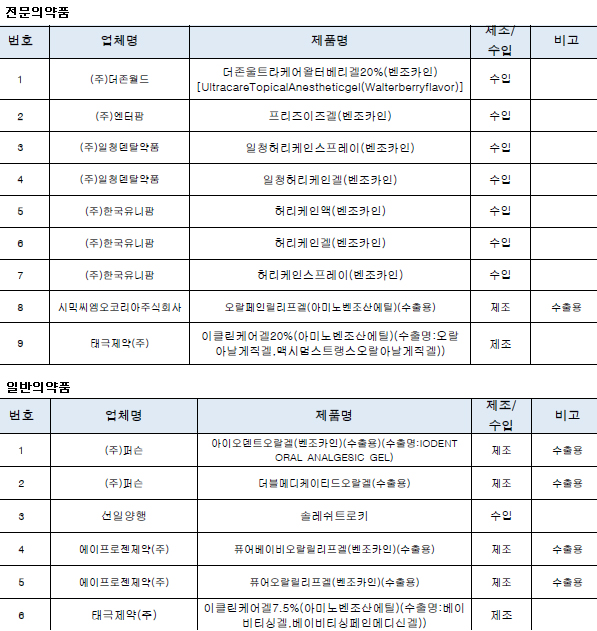
조정희 기자
news@pharmstoday.com

