아베식스, 유전자 치료제 ‘AVXS-101’ 접근…효과적 약품 시급
바이오젠은 진행성 질병의 다양한 유형이 있는 환자에게 효과를 보인 만성 치료제인 RNA 약품 스핀라자(Spinraza, nusinersen)를 SMA 치료에 처음으로 출시했다.
그러나 획기적 약품의 매출은 둔화되고 있고 노바티스가 87억달러에 인수키로 합의한 미국 유전자 치료제 개발 경쟁사인 아베식스(AveXis)로부터 압박을 받고 있다.두 회사는 최근 LA에서 열린 AAN(American Academy of Neurology) 미팅에서 각각 업그레이드된 데이터를 발표했다.
아베식스는 주요 임상 연구로부터 첫 번째 데이터와 이전 것을 업데이트한 데이터를 공개했다.바이오젠은 스핀라자의 지속 중인 오픈-라벨 확대 연구의 데이터를 제공하고 약품 매출에 보고했다.
아베식스
아베식스는 가장 심각한 SMA 1형이 있는 STR1VE 환자에 대한 정보를 처음으로 공개했다.
더 경증 SMA 유형은 독자적으로 걷고 기능하는 능력을 빼앗는다.
STR1VE은 FDA 승인 전 최종결정을 위해 기획된 주요 임상이다.연구는 총 15명 환자가 등록됐고 아베식스의 AVXS-101의 1회 치료를 받았다.
AAN에서 아베식스는 11명 환자가 4월11일부터 투약을 했고 그 중 6명은 최소 1개월 전에 유전자 치료를 받았다.이런 환자 중 6명은 연구의 목표에 도달했다.
환자들은 이동 기능을 평가하는 CHOP-INTEND 테스트에 대한 점수가 개선됐다.아베식스 치료제의 초기 연구에서 CHOP-INTEND 점수는 1개월 후 평균 9.8점, 3개월 후 15.4점까지 증가했다.
지금까지 STR1VE에서 6명 환자의 점수는 1개월 후 7.8점, 3개월 후 3명에서 17.3점까지 올랐다고 아베식스가 밝혔다.지금까지 심각한 부작용은 보고되지 않았고 2명의 환자가 문제를 유도하지 않는 간 효소 상승이 있었다.
AVXS-101의 초기 연구결과는 주목을 받고 있고 주요 안전성 문제는 아직 나타나지 않고 있다.아베식스는 최소 2년 관찰 후 환자의 결과를 AAN 미팅에서 업데이트했다.
2년 후 연구에 참가한 모두 15명 환자들은 생존하고 있고 산소호흡기가 필요 없었다.이런 환자들은 저용량 그룹은 평균 27.8개월, 고용량 그룹은 30.7개월이었다.
SMA 1형이 있는 미치료 환자의 8%가 20개월 후 생존한다고 아베식스가 밝혔다.아베식스는 SMA의 다양한 유형에 AVXS-101을 테스트하기 위해 SPRINT 연구를 시작했다.
바이오젠FDA가 스핀라자를 승인한 2016년 12월까지 SMA 치료제는 없었다.
1년에 수회 척수에 주입하는 스핀라자는 다양한 SMA 유형의 진행을 완화하고 생명을 연장해 치료의 돌파구였다.
AAN에서 바이오젠은 SHINE 이란 스핀라자 장기 연구의 결과를 업데이트했다.연구는 앞선 임상 ENDEAR에서 위약을 받은 환자와 스핀라자를 처음 받고 계속 사용하는 환자가 포함됐다.
바이오젠은 대부분 1형으로 발전되는 유아기 징후 SMA이 있는 89명 환자의 중간 데이터를 발표했다.두 그룹은 2017년 6월 30일자로 이익이 보이고 있다고 보고했다.
ENDEAR 임상에서 위약군은 평균 22.6주 후 사망했거나 산소 호흡기가 필요했다.스핀라자로 시작한 환자의 사망 혹은 산소호흡기 필요하고 약품을 계속 받는 평균 시간은 73주였다.
위약으로 시작하고 스핀라자로 전환한 환자들은 평균 9.2개월 악화되지 않았다.스핀라자 실적
스핀라자는 바이오젠의 최대 혹은 가장 수익성 높은 약품은 아니지만 작년 회사 실적의 중요한 부분이 빠르게 됐다.
그러나 작년 4분기 3.63억달러에 비해 제자리 성장에 머물렀다.
1분기 미국과 국제 시장에서 스핀라자는 각각 1.88억달러, 1.76억달러의 매출을 기록했다.같은 시장에서 2018년 1분기 스핀라자는 전분기에 비해 각각 14% 감소와 22% 성장을 했다.
미국에서 하락의 최대 이유는 치료를 시작하는 새로운 환잣수 감소이다.1분기 새로운 환자는 280명으로 전분기 420명보다 크게 감소했다.
환자의 42%는 현재 유지요법을 받고 있다.바이오젠은 SMA 환자의 최대 그룹인 소아와 성인에 초점을 맞추고 있다.
바이오젠은 스핀라자의 모든 권리를 2016년 아이오니스 파마슈티컬에서 라이선스했다.최근 아이오니스와 10억달러에 10년간 계약을 연장했다.
노바티스의 아베식스 인수는 올해 중반 완료될 것으로 예상된다.노바티스는 순조롭게 진행되면 AVXS-101을 2019년 미국에서 마케팅을 시작할 수 있을 것으로 기대했다.
스핀라자와 달리 AVXS-101은 장기간 지속할 수 있는 유전자 치료제이다.파이프라인
이밖에 노바티스, 로슈 등도 SMA 약품을 연구하고 있다.
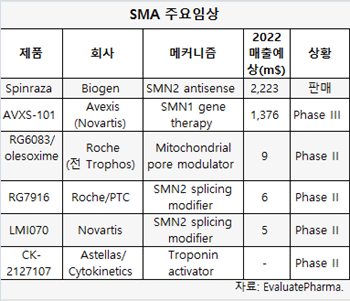
로슈는 2011년 PTC 테라퓨틱스와 제휴를 통해 SMA 약품을 개발하고 있다.
이후 2015년 개인회사인 트로포스(Trophos)를 인수해 올레소심(olesoxime)을 획득했다.올레소심은 초기에 유망함을 보였고 현재 임상 등록에 있는 올레소심과 2개 PTC 취득 자산 중 하나인 RG7916은 SMA에 현재 로슈의 주요 표적이다.
PTC 테라퓨틱스는 진행하고 있는 FIREFISH 임상에서 RG7916를 SMA 1형 환자에 평가한 예비 데이터를 AAN에서 발표했다.연구에서 모든 용량에 우수한 내약성을 보였고 중단을 유도하는 약품 관련 안전성 문제는 없었다고 보고했다.
첫 투여의 평균 나이는 6.7개월이었고 유아들은 14.8개월까지 RG7916을 받았다.아스텔라스, 카탈리스트 파마슈티컬 등 많은 바이오기업과 대학들이 SMA 치료제를 연구하고 있다.
미국 임상등록 기관인 ClinicalTrials.gov에 따르면 SAM 치료에 초기 임상 1상부터 4상까지 53건 연구가 등록돼 있다.
