총 140건 중 종근당 7건 최다…임상 1상 40건·임상 3상 35건 순
임상시험 승인 건수가 가장 많은 신청자는 종근당이었으며, 임상시험 단계별로는 1상이 가장 많았다.
3일 식품의약품안전처에 따르면 올해 1분기 임상시험 승인 건수는 총 140건으로 전년 153건 대비 약 8.5% 감소했다.신청자별로 살펴보면 종근당이 7건으로 가장 많았고, 한국얀센이 6건, 삼성서울병원과 아이큐비아(구 퀸타일즈)가 각 5건으로 뒤를 이었다.
서울대병원, 서울아산병원, 한국노바티스, 한국로슈, 한국아스트라제네카, 한국애브비 각 4건이었으며, 메디톡스, 코반스코리아서비스, 한국엠에스디, 한미약품은 각 3건으로 나타났다.이밖에 녹십자 등 18곳은이2건, 대웅제약 등 총 45곳이 각 1건의 임상시험을 승인 받았다.
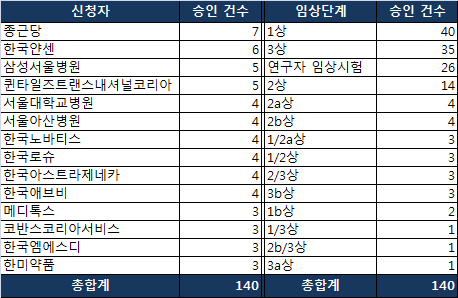
또 임상 1/2a상과 1/2상, 2/3상, 3b상이 각 3건이었으며, 1b상이 2건, 1/3상과 2b/3상, 3a상이 각 1건으로 나타났다.
국내 제약사의 주요 임상 승인현황을 보면 종근당은 CKD-330과 D150에 대한 임상 3상을 승인 받았다.CKD-330 임상은 이상지질혈증을 동반한 고혈압 환자를 대상으로 CKD-330과 D086 병용투여의 유효성과 안전성을 비교평가하기 위한 것으로, ARB 계열의 칸데사르탄과 CCB 계열인 암로디핀 복합제에 아토르바스타틴을 결합한 것이다.
또 D150과 D759 병용요법으로 혈당이 적절하게 조절되지 않는 제2형 당뇨병 환자를 대상으로 듀비에정을 추가 병용투여했을 때의 유효성 및 안전성을 비교 평가하기 위한 임상 3상을 승인 받았다.메디톡스는 양성교근비대 소견을 보이는 대상자에서 메디톡신주의 유효성과 안전성을 평가하기 위한 임상 3상을 승인 받았다.
한미약품은 건강한 성인 남성에서 HCP1303(구구탐스) 캡슐 투여와 HGP1201 정, HGP1701 캡슐 병용 투여 시의 약동학적 특성을 탐색하기 위한 예비 연구인 임상 1상을 승인 받았다.
조정희 기자
news@pharmstoday.com

