‘루센티스’ 특허 ‘아이리아’ 침해 소 제기…판도 영향은 의문
노바티스와 리제너론이 나이 관련 황반변성(AMD) 분야에서 강력한 경쟁을 하고 있다.
최근 노바티스는 라이벌 제약사 리제너론이 AMD 치료제 아이리아(Eylea)의 제조와 관련된 특허를 침해했다며 뉴욕남부지방법원에 소송을 제기했다.미국 특허 688은 포유류 세포에 폴리펩타이드의 발현에 대한 한 벡터에 적용되고 노바티스의 루센티스(Lucentis) 개발에 사용됐다.
노바티스는 아이리아와 항암제 잘트랍(Zaltrap)의 생산에 사용은 리제나론이 688 특허에 적용된 같은 기술을 이용하는 론자 그룹이 개발한 상업적 유전자 발현 시스템을 도용했다고 주장했다.리제너론은 벡터들은 바이오로직 약품들의 개발에 일상적으로 사용되고 있다고 밝혔다.
회사는 소송을 평가하고 있고 리제네론에 대한 688 특허 강제에서 노바티스에 대응하기 위해 강력한 방어를 할 것이라고 말했다.현재 노바티스는 688 특허침해에 대한 손해배상을 요구하고 있다.
리제너론은 이번 소송에 대해 강력하게 방어할 예정이라고 밝혔다.임상 경주
강력한 경쟁에도 노바티스는 루센티스를 지키기 위해 고군분투했다.
작년 11월 노바티스는 아이리아와 비교한 브로루시주맙(brolucizumab)의 임상 3상 결과를 발표했다.
임상에서 브로루시주맙은 연구의 1차 목표인 AMD 환자에서 최대 교정시력(best-corrected visual acuity)의 심한 변화에 비열등을 입증했다.노바티스는 HAWK, HARRIER 등 2개 직접비교 임상을 실시했다.
16주에서 아이리아와 비교해 35% 더 낮은 브로루시주맙 6mg 환자들은 HAWK에서 IRF(intra-retinal fluid)와 SRF(sub-retinal fluid)의 존재를 보였고 HARRIER에서는 33% 더 낮았다.노바티스의 브로루시주맙이 FDA 승인을 받으면 아이리아와 강력한 경쟁이 예상된다.
최근 리제너론은 임상 3상 PANORAMA 연구의 결과를 발표했다.연구는 비증식성 당뇨망막증의 치료에 아이리아의 안전성과 효능을 평가했다.
PANORAMA 임상에서 24주 아이리아 치료 환자들 사이에서 58%가 DRSS(Diabetic Retinopathy Severity Scale)는 기준선에서 2단계 이상 개선을 보인 반면 위약군은 6%였다.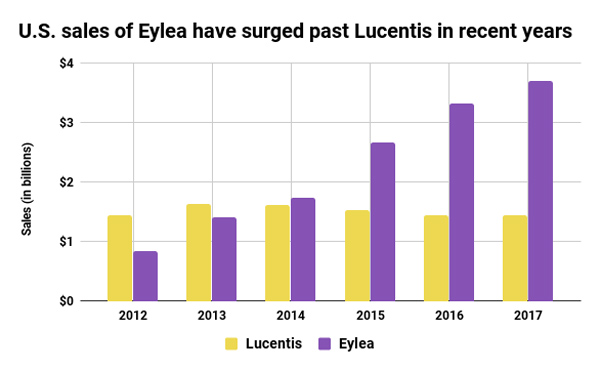
루센티스는 습성 AMD의 치료에 2006년 미국 FDA에서 처음 승인을 받았다.수년간 시장에서 경쟁 약품이 없었다.
루센티스는 AMD와 다른 유리체 장애의 치료에 유일하게 승인된 단백질 기반 치료제였다.
이후 리제너론의 아이리아가 2011년 승인됐다.리제너론의 아이리아가 루센티스를 매출에서 앞지르는데는 오래 걸리지 않았다.
리제너론은 미국에서 아이리아를 판매하는 반면 바이엘이 미국 이외에서 마케팅하고 있다.2017년 4분기 아이리아의 글로벌 매출은 16억달러로 전년대비 19% 급증했다.
4분기 미국 매출은 9.75억달러로 전년동기대비 14% 성장했다.2017년 아이리아의 총매출은 59억달러로 전년 52억달러보다 증가했다.
미국 매출은 37억달러로 11% 성장했다.바이엘은 미국 이외에서 아이리아의 2017년 매출은 14억 유로로 전년대비 15.7% 증가했다고 보고했다.
루센티스는 미국 이외에서 노바티스, 미국은 로슈가 마케팅하고 있다.작년 4분기 노바티스의 루센티스 매출은 4.85억달러로 전년동기대비 7% 성장했다.
노바티스는 2017년 루센티스의 매출은 19억달러로 전년대비 3% 증가했다고 밝혔다.로슈의 작년 루센티스 미국 매출은 14억 프랑(CHF)로 1% 늘어났다고 보고했다.

