소규모·중복 임상 한계…산·학·정, 협력 효율 증가
새로운 면역요법제 개발을 위한 경주는 항암제 파이프라인에서 최대 관심사이고 전례없는 급증을 보이고 있다.
비이익 CRI(Cancer Research Institute)의 Aiman Shalabi 연구팀이 ESMO(European Society for Medical Oncology)와 Annals of Oncology 저널에 발표한 데이터를 보면 현재 2004개 면역항암제가 개발 중에 있다.면역요법제는 임상 개발 단계에 940개, 전임상 단계 1064개가 있다.
특히 PD-1/L1 약품은 임상에 50개와 5개 판매 등 파이프라인에 164건이 있다.암백신은 334건이 인간임상 중이고 224개는 임상 단계 세포치료제이다.
온콜리틱 바이러스(oncolytic viruses)는 암젠의 T-Vec에 이어 69개가 임상개발에 있고 95건은 전임상에 있다.임상 개발에 있는 T 세포 표적 면역조절제는 99건이고 전임상 개발은 199건이다.
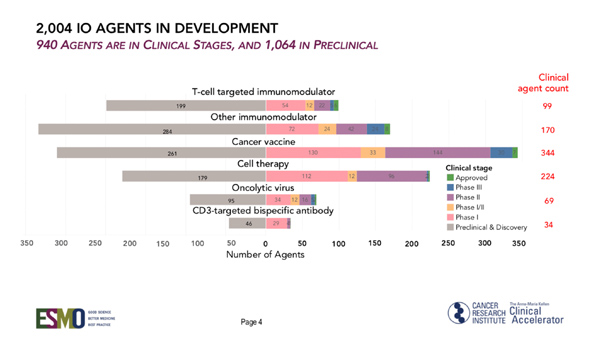
올해에만 469건의 임상시험이 5만 2539명을 대상으로 시작됐다.
연구팀은 이 분야는 매우 유망하고 많은 암 종류의 표준치료를 변경할 많은 잠재적 혁신을 전달하지만 매우 복잡하고, 세분화됐고, 중복돼 있다고 지적했다.면역요법에서 급증하는 전임상과 임상단계 프로그램의 증가는 현재 개발 중인 각각 인간 연구의 본질적 가치에 대한 심각한 의문이 높아지고 있다.
1105건 PD-1/L1 약품 연구 중 60%는 소규모, 비산업 지원 임상이다.연구팀은 단일 센터 연구과 다양한 업체에서 표적을 삼은 같은 바이오로직컬의 추적 등 전통적 임상 디자인에서 분명한 한계가 있다고 지적했다.
면역요법 전망에서 효율성을 촉진의 필요성이 시급하다고 강조했다.연구팀은 “대학, 산업, 당국, 비이익 조직이 협력은 조만간 환자에게 면역항암제의 약속을 지키는 최상의 방법이 될 수 있다”고 말했다.
고재구 기자
news@pharmstoday.com

