‘옵디보’ ‘키트루다’ ‘아벨루맙’ 말기 단계 경쟁
폐암에 대해 경쟁하는 항 PD-1/PD-L1 항체 사이의 강력한 라이벌은 다른 고형암에 대한 개발을 무색하게 하고 있다.
이는 진행성 위암에 BMS의 체크포인트 억제제 옵디보(Opdivo)의 첫 긍정적 임상 3상의 발표에 뒤이어 변할 수 있다.BMS와 파트너인 오노제약이 실시한 ONO-4538-12 연구는 작년 11월 1차 목표에 도달한 것으로 이미 보고됐다.
그러나 지금까지 자세한 데이터는 발표되지 않았다.19일부터 샌프란시스코에서 열린 미국임상종양학회(ASCO) 소화기암 심포지엄에서 자세한 데이터를 공개됐다.
493명 환자에 대한 연구는 표준요법으로 치료가 어렵거나 내성이 있는 이전 치료받은 진행성 혹은 재발 위암 환자의 생존 개선을 보인 첫 체크포인트 억제제이다.옵디보는 사망 위험을 37%, 질병 진행 위험을 40% 감소한 것을 발견했다.
하지만 매우 빈약한 진단 환자 그룹에서 이익의 절대 수준은 중앙 전체 생존은 단지 1.2개월과 진행없는 생존은 5일 이하로 미미했다.그렇지만 연구는 당국 승인 신청 기준은 물론 더 초기 단계 위암에 대한 연구에 추가 투자의 명분을 분명하게 형성할 수 있을 것이다.
임상은 PD-L1 발현의 수준을 근거로 결과를 분석하지 않았고 옵디보는 더 낮은 것보다 더 높은 발현자에게 더 큰 영향을 줄 수 있다.최근 MSD의 키트루다(Keytruda)가 1차라인 세팅에서 옵디보를 앞선 비소세포폐암은 BMS의 또 다른 문제이다.
BMS와 오노는 위암에 치료에 옵디보의 3개 대규모 연구를 진행하고 있다.하나는 1차라인으로 옥살리플라틴+플루오로피리미딘(oxaliplatin+fluoropyrimidine)에 대한 여보이와 이중 체크포인트 차단제를 복합한 임상 3상인 Checkmate-649 연구이다.
오노는 S-1(tegafur-gimeracil-oteraci) 혹은 카페시타빈+옥살리플라틴(capecitabine+oxaliplatin)의 표준화학요법에 대한 수술 후 보조요법에 위약군대 옵디보의 임상 3상에 등록을 시작했다.BMS는 옵디보와 시험 중인 항-Lag3 항체 BMS-986016를 옵디보+여보이를 비교하는 Fraction-GC 연구의 대규모 임상 2상을 실시하고 있다.
그러나 위암에 대한 다른 체크포인트 차단제에 대한 BMS의 유리함은 단축될 수 있다.독일 머크와 화이자는 Javelin Gastric 300 연구에서 3차 라인으로 아벨루맙(avelumab)을 테스팅하고 있다.
다른 아벨루맙의 연구인 Javelin Gastric 100은 1차라인 유지요법에 진행 중이다.MSD는 키트루다를 2차 라인 환자에 대한 Keynote-061 연구와 1차 라인 환자에 대한 다른 연구를 실시하고 있다.
아스트라제네카와 로슈는 각각 두발루맙(durvalumab), 티쎈트릭(Tecentriq)를 위암에 등록한 연구는 없다.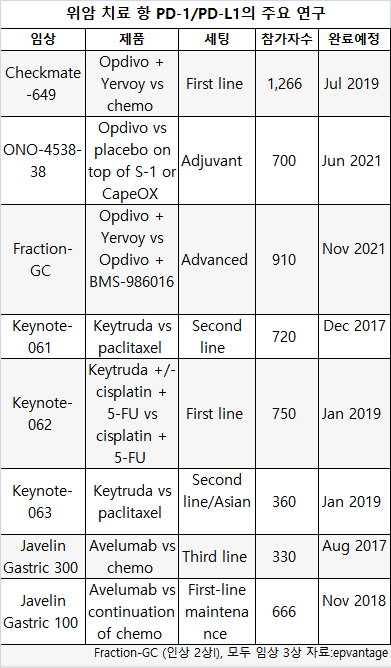
고재구 기자
news@pharmstoday.com

